Des plantes biotech au service de la santé du végétal et de l'environnement
Les plantes transgéniques, outils de la santé du végétal
Des événements de transformation pour améliorer la santé du végétal
Le développement de la culture des plantes biotech: une épopée sur vingt ans
Les promesses des nouvelles biotechnologies (NBT) pour la santé végétale
OGM et OGE végétaux: outils pour One Health, un monde, une seule santé
Un cas d’école: le maïs Bt MON 810 et le risque mycotoxines
Faire face au réchauffement climatique
Amélioration de la santé environnementale
Amélioration des itinéraires techniques phytosanitaires
Diminution du gaz à effet de serre CO2
Augmentation de la biodiversité
Les risques de dissémination par flux de gènes
Prévenir les résistances
Conclusion
Résumé
Les méthodes de modification du génome sont intimement liées à l’histoire de l’humanité, des premiers balbutiements de l’agriculture au néolithique en passant par le développement des thérapies géniques. Aujourd’hui, les techniques employées sont issues des biotechnologies (transgénèse, mutagénèse ainsi que les nouvelles techniques d’édition du génome NBT, ou New Breeding Techniques), et suscitent un débat sociétal empreint d’inquiétude ou de rejet idéologique.
Ces craintes sont-elles fondées ? Les avancées scientifiques que propose cette approche biotechnologique méritent d’être prises en considération, tout particulièrement en matière de santé.
Aujourd’hui, la mondialisation a souligné que les santés, qu’elles soient humaine ou animale, végétale ou environnementale, sont interdépendantes et réunies sous le concept One Health : une seule santé, un seul monde.
Après avoir situé les modifications du génome dans le contexte de la vie sur notre planète et les progrès qu’elles offrent en matière de santé humaine et animale ainsi que les espoirs que ces techniques suscitent, nous examinerons dans cette note les innovations qui relèvent du domaine de la santé du végétal et quelles sont les conséquences environnementales que posent réellement les plantes biotechnologiques.
Catherine Regnault-Roger,
Professeure des universités, membre de l'Académie d'agriculture de France.
Professeur des universités émérite de l’université de Pau et des Pays de l’Adour (Iprem UMR CNRS 5452 -e2S UPPA), membre de l’Académie d’agriculture de France, membre correspondant de l’Académie nationale de pharmacie, membre du comité scientifique du Haut Conseil des biotechnologies.
Dans l’étude Des outils de modification du génome pour la santé humaine et animale1, il a été rappelé que la modification du génome est un des moteurs de l’évolution sur terre et que les techniques de modification du génome sont intimement liées à l’histoire de l’humanité : du passé lointain avec les débuts de l’agriculture et la domestication des espèces, aux récents développements des techniques d’édition du génome qui ouvrent d’immenses perspectives en matière de thérapies géniques, de maîtrise des maladies vectorielles tropicales transmises par les moustiques, ou encore d’épizooties2 ainsi que d’amélioration du bien-être animal.
Qu’en est-il de la santé du végétal qui est, tout comme la santé humaine et la santé animale, un des volets importants de la santé considérée dans la globalité du concept One Health ? Et quelles en sont les conséquences pour l’environnement ? Voici quelques-unes des questions auxquelles nous allons tenter d’apporter des éléments d’information à partir des réalités scientifiques.
Les plantes transgéniques, outils de la santé du végétal
Voir Zhang Tao et Zhou Shundong, « L’utilisation des OGM en Chine : enjeux et débats », Perspectives chinoises, n° 76, mars-avril 2003 p. 52-60; Clive James, « Global Status of Transgenic Crops in 1997 », ISAAA Briefs, no 5, 1997.
Voir ainsi les nombreux dossiers spéciaux publiés dans les années 1990 par les revues La Recherche (n° 270, par exemple) ou Biofutur (n° 90 ou no 172, par exemple).
C’est en 1983 que fut obtenue la première plante transgénique dans le laboratoire belge de l’université de Gand, dirigé par Marc Van Montagu, grâce aux travaux qu’il mena avec Joseph Schnell : un tabac génétiquement modifié (GM), résultant d’un transfert de gène réalisé à l’aide d’une agrobactérie, Agrobacterium tumefaciens, privée de son gène infectieux propageant la galle du collet, une maladie des racines du végétal, pour être remplacé par un gène d’intérêt qui confère à la plante de nouvelles propriétés. Ce premier tabac biotechnologique intégrait ainsi un gène lui conférant une résistance à un antibiotique. Ce fut ensuite un tabac résistant à des insectes qui fut mis au point grâce à un transfert d’un gène du bacille de Thuringe (Bacillus thuringiensis) produisant une protéine toxique pour de nombreux insectes. Le bacille de Thuringe est une bactérie largement utilisée comme substance active insecticide incorporée dans des formulations de biopesticides (appelées aujourd’hui produits de biocontrôle) depuis plusieurs décennies, tant dans l’agriculture conventionnelle que l’agriculture biologique. Les plantes modifiées avec un gène de Bacillus thuringiensis sont appelées « Bt » (tabac Bt, maïs Bt…).
Par la suite, dans les années 1990, un plant de tabac et une tomate résistants à des virus ont été cultivés en Chine3, et, en 1994, une tomate à maturation retardée, la tomate Flavr Savr, a été commercialisée aux États-Unis pendant deux ans. Ce fut un échec commercial. Produite par la société Calgene, elle se révéla décevante tant pour ses qualités gustatives, peu convaincantes, que pour des facilités espérées dans son transport, qui ne furent pas constatées. Le rachat de Calgene par la société Monsanto en 1996 mit fin à cette expérience.
De nombreux projets de modifications génétiques sur plusieurs espèces végétales ont existé dans les cartons des laboratoires de recherche dans les années 1980-19904, mais l’essor des plantes biotech va réellement se produire à partir de 1996, avec la mise en culture de plantes transgéniques commercialisées pour faciliter le désherbage et mieux résister à des insectes ravageurs.
Quel nom pour les plantes génétiquement modifiées ?

Des événements de transformation pour améliorer la santé du végétal
Terme consacré depuis une quinzaine d’années pour désigner tout organisme nuisible à la plante.
Voir Anthony M. Shelton, Jian-Zhou Zhao et Richard T. Roush, « Economic, Ecological, Food Safety, and Social Consequences of the Deployment of Bt Transgenic Plants », Annual Review of Entomology, vol. 47, janvier 2002, p. 845-881.
Voir « ISAAA Briefs ».
Ce sont donc avec des caractères agronomiques de lutte contre les fléaux qui affectent les plantes cultivées que se sont développées les premières plantes biotech : insectes et nématodes (vers ronds) ravageurs qui attaquent la plante en train de se développer, agents pathogènes qui propagent des maladies ou encore mauvaises herbes qui sont en concurrence avec les cultures pour l’eau et les nutriments du sol dans la parcelle. En conséquence, les premières plantes transgéniques ont été modifiées pour préserver leur santé face à leurs bioagresseurs5.
C’est en 1995 que les premières autorisations de plantes GM ont été accordées aux États-Unis pour des plantes résistantes à des insectes qui leur sont nuisibles : un cotonnier (Bollgard® Cotton, portant l’événement de transformation MON 531 de Monsanto) et un maïs (Knockout® Corn, portant l’événement de transformation Bt 176 de Syngenta, tous deux résistants à des insectes de la famille des lépidoptères, ainsi qu’une pomme de terre (New Leaf Potato®, portant l’événement de transformation Russet Burbank de Monsanto) résistante à un coléoptère, le doryphore, pomme de terre également autorisée au Canada la même année6.
Grâce aux travaux de l’International Service for the Acquisition of Agri-biotech Application (ISAAA), animé pendant près de vingt ans par son fondateur Clive James, il est possible de suivre l’évolution des surfaces de plantes biotech dans le monde par culture, par transformation génétique et par pays7. Les premières mises en culture ont concerné des plantes tolérantes à des herbicides (herbicide- tolérantes, HT) et des plantes résistantes aux insectes (insectes-résistantes, IR). Dans le premier cas, on introduit dans la plante un gène qui induit la synthèse d’une enzyme qui lui permet de détoxifier cet herbicide. Si on choisit un herbicide non sélectif comme le glyphosate ou le glufosinate, seules les plantes possédant l’enzyme qui permet à la plante de résister à l’herbicide utilisé ne sont pas détruites et les autres plantes indésirables dans la parcelle le sont. Il s’agit de repousses de cultures précédentes, d’adventices ou de mauvaises herbes, comme le gaillet ou le coquelicot, qui diminuent les rendements, mais aussi des plantes délétères comme l’ambroisie ou le datura, qui sécrètent des molécules naturelles toxiques pour l’homme et les animaux. Les plantes biotech tolèrent l’herbicide qui se révèle fatal pour les autres plantes. Dans le second cas, les plantes GM contiennent des événements de transformation permettant à la plante de sécréter dans ses tissus des protéines toxiques pour des insectes qui se nourrissent de la plante. Ces insectes sont décimés par la plante, ce qui lui permet de mieux résister à leurs ravages.
Premières constructions génétiques d’un événement de transformation
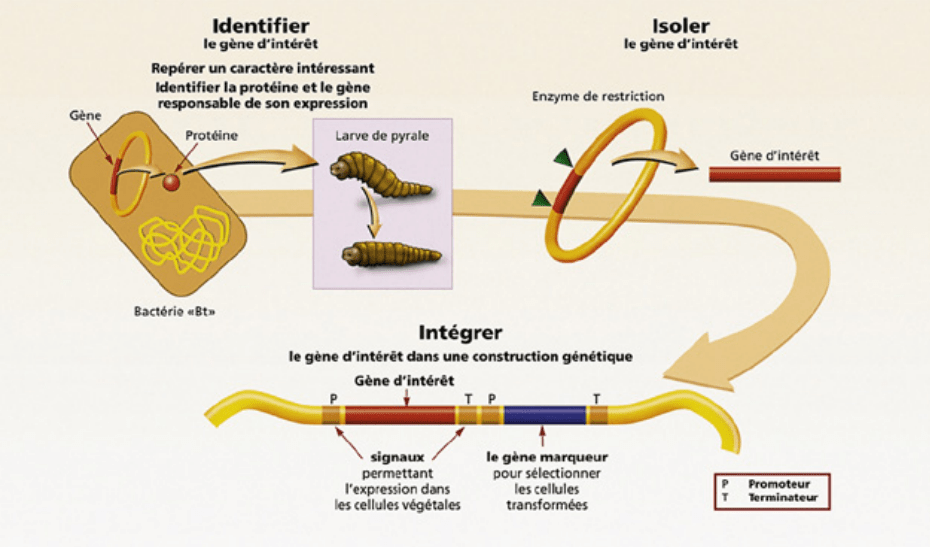
Source :
Groupement national interprofessionnel des semences et plants (Gnis), www.gnis.fr. Pour notre exemple, les gènes d’intérêts sont les gènes cry1Ab et bar, le gène marqueur est bla, auxquels s’ajoutent le gène promoteur (PEPC et spécifique du pollen 8) et un gène terminateur.
Qu’est-ce que le maïs Bt 176 Knockout® Corn ?

Le canola est produit au Canada en cultures de printemps ou d’automne : il s’agit d’un colza génétiquement modifié pour obtenir moins d’acide érucique et moins d’acides gras (AG) saturés et plus d’AG mono-insaturé (acide oléique). Voir Canola Council of Canada, « Le canola : les mythes démystifiés », canolacouncil.org (https://fr.canolacouncil.org/huile-et-tourteau/huile-de-canola/le-canola-les-mythes-démystifiés/#myth1).
Quatre cultures majeures sont concernées par les transformations biotechnologiques : le cotonnier, le soja, le maïs et le canola9 (ou colza GM cultivé au Canada). Les cultures chinoises de tabac ou de tomates génétiquement modifiées du début des années 1990 ne sont plus significatives face à cet essor. D’autres cultures nettement moins importantes vont suivre : le riz, la luzerne tolérante au glyphosate (Roundup Ready®), la papaye et la courge sont cultivés aux États-Unis, également la pomme de terre ou la betterave à sucre, ou encore l’ananas au Costa Rica et des fleurs ornementales en Colombie. Des succès sur de petites cultures localisées ont été remarqués ces dernières années : par exemple à Hawaii, avec la plantation de papayers résistants à une maladie causée par un virus, le Papaya ringspot virus (PRSV). Des espoirs sont placés dans le développement de pruniers génétiquement modifiés pour lutter contre la sharka, la maladie virale la plus dévastatrice du genre Prunus causée par le Plum pox virus (PPV). Elle a été identifiée à l’origine dans les Balkans et a fortement essaimé, notamment en Amérique du Nord. On remarque également la large adoption de l’aubergine Brinjal Bt (IR) par les agriculteurs du Bangladesh. Ils étaient vingt en 2014 et plus de vingt-sept mille en 2017, totalisant une superficie de 2 400 hectares (il s’agit de très petites exploitations) sur un total de 50 000 hectares d’aubergines cultivées.
La transformation dominante pour les quatre grandes cultures est la tolérance à un herbicide, qui surpasse encore la résistance aux insectes ou aux virus. Parallèlement se développe l’empilage de caractères, c’est-à-dire le fait que, dans une même plante, il puisse y avoir plusieurs gènes de transformation. Ainsi, si la surface consacrée à des plantes biotech tolérantes à un ou des herbicides a culminé avec 100 millions d’hectares en 2015 (et autour de 20 millions d’hectares pour les plantes biotech résistantes à des insectes et à des virus), en 2017 ce ne sont plus que 88,7 millions d’hectares qui sont consacrés à la tolérance à un ou des herbicides (HT) et 23,3 millions d’hectares à la résistance à des insectes (IR) et à des virus. En revanche, on observe un essor marqué des cultures de plantes contenant plusieurs éléments de transformation, avec une progression de plus de 50 millions d’hectares en dix ans (20 millions d’hectares en 2007 et 77,7 millions d’hectares de cultures en 2017). Ces plantes sont tolérantes à des herbicides et résistantes à des insectes et des virus (IR-HT), ce sont des plantes polyvalentes qui peuvent se défendre contre plusieurs bioagresseurs.
Le développement de la culture des plantes biotech: une épopée sur vingt ans
Voir à ce sujet , Marcel Kuntz, L’Affaire Séralini. L’impasse d’une science militante, Fondation pour l’innovation politique, juin 2019.
Voir Clive James, art. cit.
Avant de passer au stade de la commercialisation des plantes GM, de nombreuses expérimentations en champ ont été conduites pendant dix ans. Un tiers des essais concernait le maïs, un cinquième le canola, la tomate et la pomme de terre faisant jeu égal avec 11%, puis, à moins de 10%, le soja (9%), le cotonnier (7%) et le tabac (5%). Entre 1986 et 1997, ce ne sont pas moins de 25 000 essais (15 000 avant 1995, 10 000 entre 1995 et 1997) concernant 60 mises en culture, 10 caractères de transformations qui ont été conduits dans 45 pays par des sociétés qui ont déposé des dossiers de demandes d’autorisation de commercialisation (importation et mise en culture) dans plusieurs pays.
Le dialogue est alors de mise entre les autorités en charge de la réglementation et les équipes d’expérimentateurs. Les résultats sont communiqués à la communauté scientifique et au grand public pour en débattre10. L’important, selon Clive James11, est alors de contribuer à faire comprendre ce que sont les cultures transgéniques.
Après cette phase d’essais, c’est en 1996 que commencèrent réellement la mise en culture et la commercialisation des plantes biotech, dont l’essor se mesure par l’expansion des surfaces cultivées.
Ces dernières années, on note une diversification des caractères. Deux générations de pomme de terre Innate®, dont les modifications ralentissent le brunissement ou protègent contre le mildiou, ont été approuvées aux États-Unis et au Canada en 2016 et 2017, de même que les pommes Artic®, mises au point pour limiter le brunissement. Le soja Plenish™ contient plus d’acide gras insaturé (acide oléique) et moins d’acides gras saturés que le soja conventionnel, ce qui améliore le profil nutritionnel de l’huile qui en est extraite. Depuis 2013, un caractère de tolérance à la sécheresse est intégré dans les empilements de maïs et répond à une forte demande, notamment en Afrique, puisque la superficie a augmenté pour passer de 50 000 hectares en 2013 à 1,2 million en 2016 et à 1,4 million en 2017.
Évolution des surfaces biotech cultivées entre 1996 et 2017

Voir Clive James et Anatole F. Krattiger, « Global Review of the Field Testing and Commercialization of Transgenic Plants, 1986 to 1995. The First Decade of Crop Biotechnology », ISAAA Briefs, n° 1, 1996.
Voir Catherine Regnault-Roger, OGM et produits d’édition du génome (OGE) : enjeux réglementaires et géopolitiques, Fondation pour l’innovation politique, janvier 2020.
Communication personnelle d’Alain Toppan, directeur général du groupe Biogemma (2017-2018), ancien chef développement OGM Europe du groupe Limagrain puis du groupe Vilmorin (2006-2017).
Au début, la commercialisation des plantes transgéniques a été réalisée par une majorité des grandes sociétés privées (Monsanto, AgrEvo, Florigene, Calgene, SEITA, Zeneca…), mais aussi par des universités qui valorisaient les travaux de recherche de leurs laboratoires (Cornell University ou Université du Saskatchewan, par exemple12). Puis, au fil des années, des concentrations par fusion-acquisition de sociétés du secteur des semences et de l’agrochimie se sont opérées, façonnant la structuration actuelle avec trois groupes majeurs, ancrés sur trois régions différentes : Corteva Agriscience (2019) aux États-Unis (siège social au Delaware), ChemChina et sa filiale Syngenta (2017) en Chine (siège social à Pékin) et Bayer CropScience (2018), ayant absorbé Monsanto, en Europe (siège social en Allemagne). Ces consortiums ont les moyens de faire face à des réglementations de plus en plus exigeantes, tout particulièrement à celles de l’Union européenne13, réclamant des dossiers de demandes d’homologation et de suivi postcommercialisation très onéreux à constituer (plus de 100 millions d’euros par dossier14).
Concentrations par fusion-acquisition de sociétés pour former les trois grands groupes leaders du secteur agricole (agrochimie & biotechnologies)
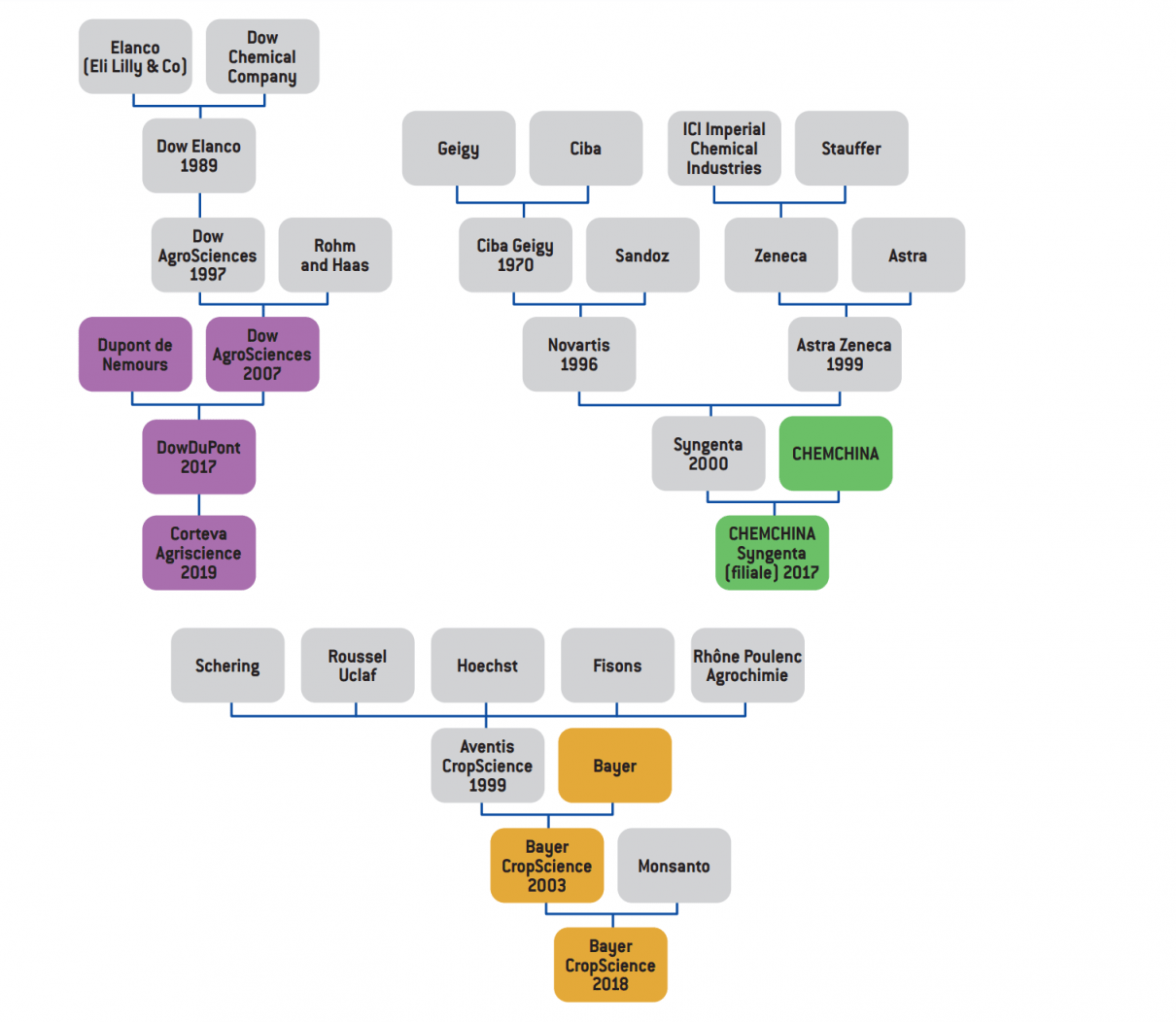
Source :
Adapté, révisé et actualisé à partir d’un schéma initialement proposé par Bernard Ambolet, « La chimie organique au service de l’agriculture », in Catherine Regnault-Roger et André Fougeroux, Santé du végétal : 100 ans déjà ! Regards sur la phytopharmacie, Presses des Mines, 2018, p. 86.
Les promesses des nouvelles biotechnologies (NBT) pour la santé végétale
Le nucléotide est l’unité de base des acides nucléiques (ADN et ARN) constituée d’une base azotée, d’un pentose et de groupes phosphates.
Transformation qui se situe à un autre endroit du génome que celui visé.
Dominik Modrzejewski et al., « What is the available evidence for the range of applications of genome editing as a new tool for plant trait modification and the potential occurrence of associated off target effects: a systematic map », Environmental Evidence, vol. 8, article n° 27, juillet 2019 (https://environmentalevidencejournal.biomedcentral.com/articles/10.1186/s13750-018-0130-6).
Les dernières techniques d’édition du génome sont plus précises, plus rapides et moins onéreuses que la transgénèse ou la mutagénèse aléatoire et ont été de ce fait très vite intégrées dans la boîte à outils des sélectionneurs de semences pour optimiser l’amélioration variétale des plantes cultivées ; c’est d’ailleurs pourquoi elles sont appelées communément « New Plant Breeding Techniques » ou NPBT (nouvelles techniques de sélection végétale).
Elles sont utilisées pour provoquer une modification de l’ADN génomique en créant des mutations ciblées par substitution d’un nucléotide15 par un autre, par une délétion ou insertion de nucléotides, ou encore en induisant des coupures de l’ADN pour y insérer un nouveau fragment. Avec certaines de ces nouvelles techniques, cette coupure est si précise qu’on parle de « ciseaux moléculaires ». Ces modifications sont très ciblées et la notion de réécriture du génome ou d’édition du génome (genome editing) s’est imposée. En effet, il ne s’agit pas de provoquer un grand bouleversement de l’ADN par l’action à l’aveugle d’un rayonnement physique et d’un agent chimique mutagène comme cela se produit dans une mutation aléatoire, ou encore de procéder à l’introduction au hasard d’un nouvel ADN dans une cellule à l’aide de diverses techniques de pénétration comme cela se fait dans une transgénèse. À ces modifications aléatoires succède une deuxième phase de tri entre plusieurs milliers de cellules obtenues afin de sélectionner celles qui portent la transformation du génome recherchée. En procédant par édition génomique, les effets hors cible16 se sont considérablement réduits et ont par conséquent diminué la phase de tri, ce qui économise du temps et de l’argent. De plus, en utilisant certaines techniques d’édition du génome, il est impossible de distinguer si l’organisme que l’on examine provient d’une manipulation génétique en laboratoire ou résulte d’une mutation spontanée intervenue dans la nature. Avec de tels outils de précision, les étapes d’une sélection végétale classique pour l’amélioration variétale se sont considérablement allégées et les recherches dans le domaine du végétal se développent intensément.
Une revue récente de la littérature scientifique recense les publications sur le sujet des NPBT entre janvier 1996 et fin mai 201817. Sur 1 328 études consacrées aux applications de l’édition du génome (genome editing) dans le domaine des plantes agricoles et modèles, la technique CRISPR, découverte en 2012, a le plus mobilisé les chercheurs : 1 032 articles lui sont consacrés. L’édition de base (base editing), la très récente technique d’édition du génome qui est mentionnée pour la première fois en novembre 2017, a déjà suscité 42 articles en six mois.
Publications de recherche consacrées aux différentes NPBT par techniques entre janvier 1996 et fin mai 2018
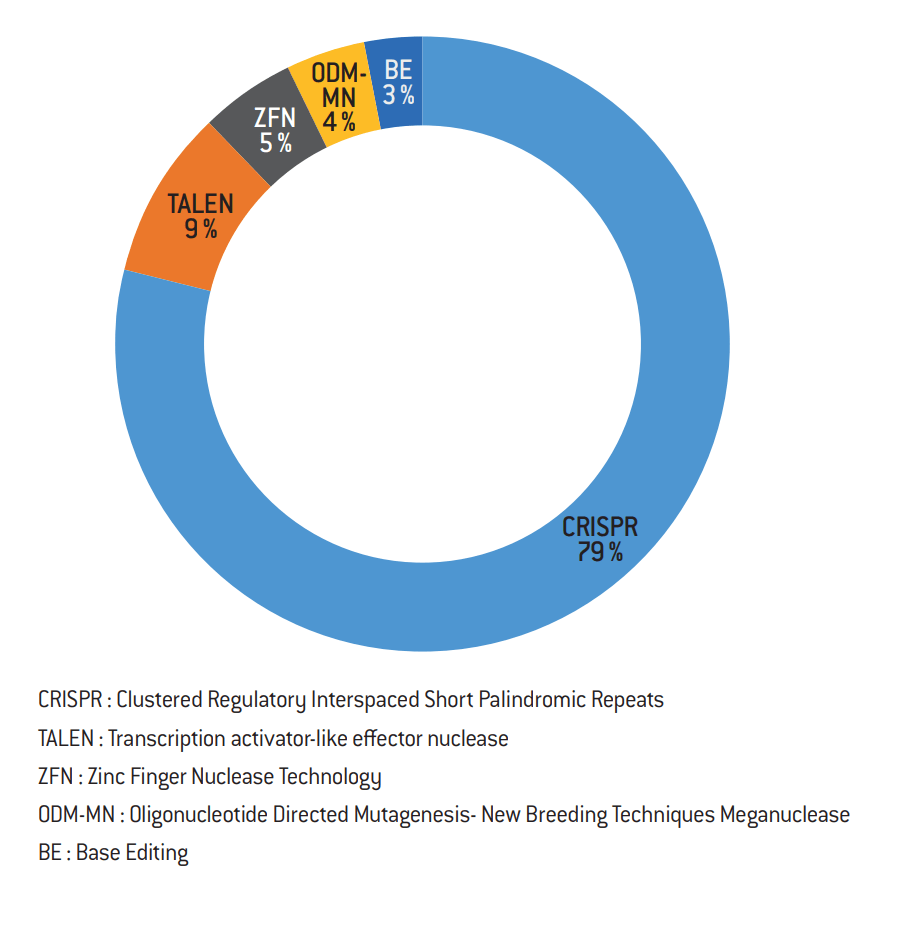
Source :
D’après Dominik Modrzejewski et al., « What is the available evidence for the range of applications of genome editing as a new tool for plant trait modification and the potential occurrence of associated off target effects: a systematic map », Environmental Evidence, vol. 8, article n° 27, juillet 2019 (https://environmentalevidencejournal.biomedcentral.com/articles/10.1186/s13750-018-0130-6).
Voir à ce sujet la troisième note de cette série : Catherine Regnault-Roger, OGM et produits d’édition du génome (OGE) : enjeux réglementaires et géopolitiques, Fondation pour l’innovation politique, janvier 2020.
Pour une définition des SDN (site directed nuclease), voir Catherine Regnault-Roger, Des outils de modification du génome au service de la santé humaine et animale, op. cit. Pour rappel : SDN1, inactivation d’un gène par coupure ciblée et réparation défectueuse (délétion ou insertion de quelques nucléotides) ; SDN2, modification ciblée de quelques nucléotides dans un gène donné ; SDN3, insertion ciblée d’un ADN étranger à un site donné.
Ces publications ont concerné vingt-huit espèces de plantes cultivées. On remarque l’importance du riz, ce qui ne surprend pas quand on sait que le continent asiatique a piloté à lui seul plus de 50% de ces publications de recherche18. La deuxième plante la plus étudiée est la plante modèle Arabidopsis taliana, l’Arabette des dames. Les organismes modèles sont étudiés par toute la communauté scientifique internationale et donnent des points de repères en matière d’avancées scientifiques.
Sur l’ensemble des projets de recherche, 99 portaient sur des applications commerciales ou industrielles directes pour améliorer (par ordre décroissant) :
- des caractères agronomiques (itinéraires techniques, croissance, rendement) : 38% ;
- la qualité alimentaire (nutrition humaine et animale) : 28% ;
- la tolérance aux stress biotiques (insectes ravageurs, maladies, virus, etc.) : 16% ;
- la tolérance aux stress abiotiques (sécheresse, carence en azote, rayonnements UV, etc.) : 5% ;
- la tolérance à des herbicides : 8% ;
- la valorisation industrielle : 5%.
Les techniques de transformation sont très majoritairement des modifications mineures de type SDN1, point de mutation ou édition de base (92%). Pour les modifications du génome plus conséquentes, 3% sont classées en SDN2 et 5% en SDN319.
Espèces végétales étudiées par NPBT (entre janvier 1996 et fin mai 2018), par importance décroissante du nombre de publications de recherche dédiées
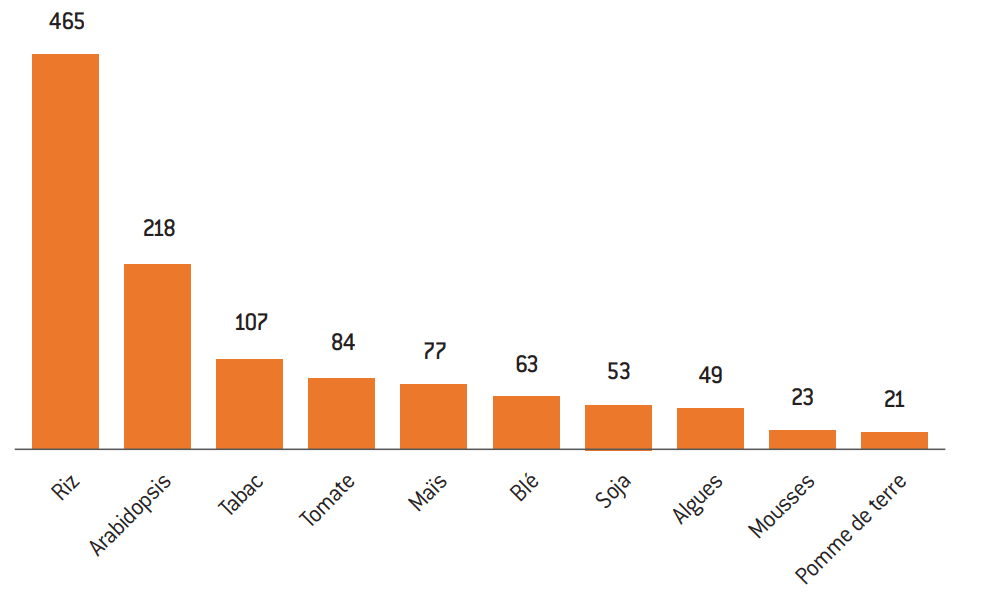
Source :
D’après Dominik Modrzejewski et al., art. cit.
Les recherches se sont déroulées dans 68 pays, et deux d’entre eux sont particulièrement actifs : la Chine (599 publications, soit 40%) et les États-Unis (487 publications, soit 33%). Parmi les laboratoires et sociétés très en pointe sur ces recherches, on note un fort investissement des organismes chinois (Académie des sciences de Chine et les académies d’agriculture de diverses provinces ainsi que des universités chinoises), non seulement pour les études sur le riz pour lesquelles ils déploient des activités intenses mais aussi sur le colza, le cotonnier, la tomate et le blé. La Chine est leader pour les applications agricoles.
De nombreuses universités américaines (Californie, Minnesota, Florida, Kansas State, Penn State), quelques universités au Japon (Tamagawa, Tsukuba, Tosushima) et en Europe (université de Kiel en Allemagne, université Paris- Saclay et de Montpellier en France) ou des centres de recherche bien connus comme l’Institut des sciences Weizmann en Israël ou l’Institut Max-Planck en Allemagne ou l’Instituto de Agricultura Sostenible du Consejo Superior de Investigaciones Científicas (CIC) en Espagne, ainsi que des sociétés du secteur privé (DuPont-Pioneer, Syngenta seeds, Cellectis Plant Sciences, Calyxt, Dow AgroScience) sont très engagés dans ces recherches.
OGM et OGE végétaux: outils pour One Health, un monde, une seule santé
Voir Catherine Regnault-Roger, Des outils de modification du génome au service de la santé humaine et animale, op. cit.
Comme nous l’avons vu dans la première note de cette série20, en préservant la santé des humains et des animaux, nous préservons la santé du monde car, dans le cadre du concept One Health, il n’y a qu’un seul monde et une seule santé. La santé du végétal s’inscrit pleinement dans ce concept, et les OGM et OGE illustrent parfaitement qu’en améliorant la santé du végétal avec les biotechnologies végétales, on a la possibilité d’améliorer la santé de tous.
Un cas d’école: le maïs Bt MON 810 et le risque mycotoxines
Laurent Folcher et al., « Lower mycotoxin levels in Bt maize grain », Agronomy for Sustainable Development, vol. 30, n° 4, décembre 2010, p. 711-719.
Le maïs Bt MON 810, la seule plante transgénique cultivée dans l’Union européenne (essentiellement aujourd’hui en Espagne et un peu au Portugal), est un cas d’école. Ce maïs est génétiquement modifié par incorporation d’un gène qui permet aux cellules de la plante de synthétiser une protéine à caractère insecticide. Celle-ci perturbe le fonctionnement digestif de deux ravageurs majeurs de cette culture, la pyrale du maïs (Ostrinia nubilalis) et la sésamie (Sesamia nonagrioides). Les variétés de maïs MON 810 les contrôlent efficacement en diminuant les populations de ces insectes de plus de 90% dans les parcelles cultivées21. Outre la limitation des dégâts des insectes sur les épis et les tiges de maïs, ce maïs transgénique développe un effet bénéfique dans les régions où sévissent des fusarioses, maladies affectant la santé du maïs.
À un stade avancé, les épis de maïs se couvrent de moisissures, symptôme de l’installation des champignons pathogènes, des Fusarium agents de cette maladie. Les fusarioses s’accompagnent, dans des conditions environnementales favorables pour leur développement, de production de mycotoxines (toxines produites par des champignons) extrêmement dangereuses et délétères qui contaminent les récoltes.
Selon la nature des mycotoxines produites, différentes pathologies peuvent survenir chez l’homme ou chez l’animal : atteintes rénales, du foie, du tube digestif, du système immunitaire et de l’appareil reproducteur. Certaines mycotoxines sont cancérogènes, d’autres sont des perturbateurs endocriniens. Des maladies sévères ont été constatées chez les humains à la suite de consommation de farines contaminées. Dans notre mémoire historique figure encore, au Moyen Âge, le mal des Ardents ou feu de saint Antoine qui provoquait des hallucinations et des troubles circulatoires pouvant aller jusqu’au décès, ou encore, dans les années 1950, la consommation de pain à Pont-Saint-Esprit qui se soldera par la mort de dix personnes et une cinquantaine d’internements psychiatriques.
Épis de maïs d’une parcelle expérimentale cultivée avec des maïs Bt et conventionnels

Source :
Catherine Regnault-Roger, photos prises en Espagne en 2010.
Voir Catherine Regnault-Roger, « Comment prévenir le risque de mycotoxines dans la production agricole ? », Science & Pseudo-Sciences, n° 322, octobre-décembre 2017, p. 45-48.
Voir Catherine Regnault-Roger et Marc Delos, « L’intérêt des plantes génétiquement modifiées pour la production agricole : le cas du maïs Bt », in Agnès Ricroch, Yves Dattée et Marc Fellous (dir.), Biotechnologies végétales. Environnement, alimentation, santé, Vuibert, 2011, p. 200-211.
Voir Filippo Rossi, Mauro Morlacchini, Giorgio Fusconi, Amedeo Pietri et Gianfranco Piva, « Effects of insertion of Bt gene in corn and different fumonisin content on growth performance of weaned piglets », Italian Journal of Animal Science, vol. 10, n° 2, 2011, p. 95-100.
L’alimentation animale n’est pas en reste. Des chevaux ont ainsi été intoxiqués par des fourrages ou des litières contaminés par ces mycotoxines et les éleveurs de cochons connaissent bien les troubles gastro-intestinaux et de la croissance qu’occasionnent à leurs animaux des lots de céréales contaminées. En 1960, des élevages de dindons britanniques ont été décimés par des arachides importées du Sénégal et contaminées par des aflatoxines sécrétées par un champignon s’épanouissant en milieu tropical, l’Aspergillus22. La prise de conscience du risque mycotoxines a conduit les autorités sanitaires européennes à établir une réglementation en 2007 fixant des seuils à ne pas dépasser.
Des travaux de recherche ont montré que la transformation génétique dont bénéficie le maïs Bt MON 810 diminue non seulement le nombre des insectes ravageurs, qui sont décimés par la toxine Bt après consommation des tiges ou épis, mais aussi les teneurs en mycotoxines dans les récoltes23. En effet, la diminution des insectes phytophages conduit à la réduction du nombre de blessures qu’ils infligent à la plante en se nourrissant et par lesquelles s’installent les champignons pathogènes agents des fusarioses et producteurs de mycotoxines.
La culture du maïs MON 810, en diminuant l’incidence de fusarioses et le risque mycotoxines, bonifie la qualité sanitaire des récoltes, ce qui n’est pas sans conséquence sur la santé animale qu’elle préserve. Une étude italienne a démontré que des porcelets nourris avec du maïs contaminé par des mycotoxines avaient une perte de poids significative par rapport à ceux alimentés avec du maïs transgénique Bt MON 81024.
Faire face au réchauffement climatique
Voir Catherine Regnault-Roger, « Interdiction du maïs Bt MON 810 en France : un vrai risque pour la sécurité alimentaire », La Revue de l’Académie d’agriculture de France, n° 5, janvier 2015, p. 19-21 (numéro téléchargeable sur le site www.academie-agriculture.fr/publications/revue-aaf?page=1).
Voir Bulletin de santé du végétal maïs. Région Centre-Val de Loire, n°16 bilan, 30 octobre 2018.
Le risque mycotoxines est un risque émergent en Europe, aggravé par le réchauffement climatique. En effet, aux champignons toxinogènes classiques du genre Fusarium s’ajoute, à la faveur d’étés très chauds, l’installation de champignons qui prolifèrent normalement dans les pays tropicaux comme les dangereux Aspergillus (mentionnés précédemment à propos d’arachides) sécrétant des aflatoxines. Ainsi, au cours de ces dernières années, plusieurs contaminations par des mycotoxines de produits commercialisés ont été constatées, ce qui aurait pu avoir des conséquences dramatiques sans la vigilance des services de contrôle sanitaire.
En 2013, du lait importé d’Europe de l’Est a été refusé en France en raison de fortes teneurs en mycotoxines : les vaches avaient consommé des fourrages contaminés par des moisissures. En mai 2014, ce sont des galettes de maïs bio Auchan et du son de blé Bio-Village de la marque Repère (Leclerc) qui sont retirés en hâte des rayons des supermarchés en raison de teneurs d’une mycotoxine (le DON ou déoxynivalénol) au-delà des seuils réglementaires. En juin 2014, le journal italien Il Fatto Quotidiano a rapporté le scandale de la commercialisation de meules d’un fromage italien très apprécié, le parmesan, contaminé aux aflatoxines : scandale car il semblerait que les fromagers aient négligé la contamination du lait qui servait à faire le fromage (des arrestations ont été opérées). Cette contamination résultait des étés caniculaires de 2012 et 2013 au cours duquel les vaches avaient été nourries avec du maïs grain ou de l’ensilage contenant des champignons Aspergillus. Les autorités des différents pays européens ont pu ainsi constater à cette occasion que, lors de conditions climatiques favorables, ces Aspergillus qui sévissent de manière endémique en Afrique, contaminant les récoltes de céréales mal conservées pouvaient proliférer sur le maïs dans le sud ou l’est de l’Europe. Cet exemple démontre qu’en préservant la santé du végétal, en le protégeant de ses bioagresseurs, on diminue les risques pour la santé animale et la santé humaine. Le maïs MON 810 se révèle être un outil efficace pour la santé dans son concept One Health. Dans ces conditions, il a semblé surprenant, du point de vue scientifique et de la santé publique, que la France interdise en 2014 par la loi 2014-567 la culture des maïs génétiquement modifiés sur son sol25.
Amélioration de la santé environnementale
Amélioration des itinéraires techniques phytosanitaires
Une des conséquences logiques de l’amélioration génétique des végétaux cultivés visant à leur conférer une meilleure aptitude à limiter les effets de leurs bioagresseurs est une adaptation dans l’utilisation des produits de traitement que sont les insecticides, les fongicides et les herbicides pour la conduite des cultures et diminuer les traitements de confort, c’est-à-dire l’administration à titre préventif.
La prévention dans la conduite des cultures est en effet une spéculation sur un futur qui ne se produit pas toujours : dans certains cas, on gagne en empêchant une infestation de prendre de l’ampleur ; dans d’autres, on traite pour rien, car la météorologie a changé ou bien les conditions d’installation du parasite ne sont plus réunies. C’est là où se situe le savoir-faire d’un agriculteur : avec les technologies qu’il a à sa disposition, savoir traiter au bon moment, au bon endroit et à la bonne dose.
Avec les plantes biotech, les itinéraires techniques phytopharmaceutiques se sont donc modifiés. Pour reprendre notre exemple, une culture de maïs Bt MON 810 dispense d’utiliser des pulvérisations d’insecticides contre la pyrale et la sésamie. En produisant la protéine insecticide Cry1Ab de manière continue, le maïs est mieux protégé à tous les stades de son développement. Cette réduction d’insecticides sera d’autant plus sensible dans les régions où plusieurs générations de pyrale ou de sésamie se succèdent la même année. En France, ce phénomène était traditionnellement très présent dans les régions méridionales au climat chaud, et moins dans les régions plus septentrionales, particulièrement en Alsace, dans lesquelles la pyrale développe une seule génération par an. Mais le changement climatique est en train de bouleverser la donne. Un bulletin publié par la chambre régionale d’agriculture du Centre-Val de Loire de l’automne 2018 décrit des cas de deux générations annuelles de pyrale du maïs au lieu d’une, dans la Champagne beauceronne et la Sologne-Val de Loire, la Touraine (mais pas en Beauce-Perche ou dans le Gâtinais). La sésamie, autrefois absente, y est capturée régulièrement depuis 2010 et son aire de répartition s’étend depuis 2016 au nord de la Loire26. Le renouvellement rapproché de ces insectes ravageurs nécessite alors plusieurs traitements au cours de la saison. Avec le maïs Bt MON 810, rien de tel puisque la plante se protège elle-même27. L’économie en insecticides qui en résulte diminue les risques de résidus de pesticides dans les aliments et améliore la sécurité alimentaire. Elle présente également des avantages écologiques en abaissant les risques de contaminations de pesticides dans la biosphère28, ainsi que les émissions de gaz à effet de serre liés aux passages des engins agricoles dans les parcelles pour les traitements. Elle se traduit également par des avantages économiques en réduisant le coût des intrants et le temps de travail de l’opérateur agricole.
Diminution du gaz à effet de serre CO2
Graham Brookes et Peter Barfoot, « Farm income and production impacts of using GM crop technology 1996-2016 », GM Crops & Food, vol. 9, n° 2, 2018, p. 59-89.
Les avantages écologiques décrits ci-dessus à propos du maïs MON 810 concernent toutes les cultures GM. Au Royaume-Uni, deux experts en économie appliquée aux biotechnologies établissent annuellement un bilan annuel de l’impact environnemental de cultures biotech. Ils ont évalué que le développement actuel de ces cultures (pour rappel, une surface de 191,7 millions d’hectares en 2018) permet dans sa globalité de diminuer l’émission du gaz à effet de serre CO2 de 27,1 millions de tonnes. Cette économie est liée aux changements des pratiques agricoles (réduction des pulvérisations d’insecticides et d’herbicides pour 2,9 millions de tonnes de CO2) et aux techniques culturales simplifiées (TCS) qui diminuent la quantité de carburant consommée par les machines agricoles (économie de 24,2 millions de tonnes de CO2). Les TCS s’accompagnent en outre d’une moindre vulnérabilité des sols à l’érosion et d’une augmentation de la biodiversité tellurique (vers de terre, insectes du sol comme les collemboles).
La réduction de substances actives consommées lors des traitements insecticides et herbicides a également été calculée. Sur une période de vingt et un ans (depuis 1996), elle est évaluée à 671 millions de kilogrammes29. À cette évaluation s’ajoute un indicateur, le quotient de l’impact environnemental (Environmental Impact Quotient, EIQ) établi pour chaque substance active phytopharmaceutique dans les champs. Les auteurs constatent une amélioration de ce quotient autour de 18,5%, ainsi qu’une diminution de 8% des quantités de pesticides utilisés. Les itinéraires techniques phytopharmaceutiques se sont améliorés et sont devenus plus vertueux.
Augmentation de la biodiversité
Bernard Le Buanec, « La diversité génétique en agriculture », in Catherine Regnault-Roger (dir.), Idées reçues et agriculture. Parole à la science, Presses des Mines, 2018, p. 169-187.
Voir Jean Claude Pernollet, « Plantes génétiquement modifiées », in Catherine Regnault-Roger (dir.), Idées reçues et agriculture…, op. cit., p. 188-204.
Voir Geneviève De Lacour, « Le coton GM favorise la biodiversité, selon une étude chinoise », journaldelenvironnement.net, 15 juin 2012.
Voir Daniel Cadis, « Claude Ménara : “Mon maïs transgénique est le plus écologique !” », lefigaro.fr, 6 avril 2007.
Une autre conséquence de la culture des plantes biotech est de favoriser la biodiversité agricole. La commercialisation des plantes GM s’est traduite par une augmentation du nombre de variétés cultivées. Bernard Le Buanec, de l’Académie d’agriculture de France, donne à ce propos quelques chiffres : 87 variétés différentes de maïs Bt incluant l’événement de transformation MON 810 ont été cultivées sur 35 000 hectares en Catalogne en 2016 ; en Inde, il est dénombré 205 variétés de coton cultivées incluant l’événement de transformation MON 531 et 309 variétés pour la modification MON 1598530. De son côté, Jean-Claude Pernollet, également membre de de l’Académie d’agriculture de France, mentionne plus de 4 300 variétés de maïs transgéniques commercialisées sous 202 marques différentes et produites par 173 entreprises 31.
La lutte contre les maladies contribue aussi à sauver la biodiversité locale par la préservation déjà évoquée d’espèces conventionnelles menacées, à l’instar des pruniers sauvés de la sharka et des papayers d’Hawaii protégés du Papaya ringspot virus (PRSV).
On observe aussi la préservation des insectes bénéfiques pour les cultures (entomofaune auxiliaire) sur les parcelles cultivées avec une plante transgénique : l’épandage d’un insecticide tue la plupart des insectes du champ, tandis que la plante biotech ne tue que ceux qui s’attaquent à elle en les empoisonnant. Une augmentation de la biodiversité sur des parcelles de cotonnier GM a ainsi été observée en Chine : si les dégâts de la noctuelle du cotonnier ont bien été réduits grâce à la toxicité que manifeste la plante envers cet insecte, la réduction des insecticides a favorisé l’augmentation des populations de trois groupes majeurs d’insectes auxiliaires que sont les coccinelles, les araignées et les chrysopes32. Une constatation de même nature a été réalisée par Claude Menara33, agriculteur du sud-ouest de la France (Lot-et-Garonne), quand il cultivait du maïs MON 810 sur son exploitation avant l’interdiction de 2014.
Les risques de dissémination par flux de gènes
Jean Claude Pernollet, art. cit., p. 195.
André Gallais, « La principale variété de blé “bio” serait-elle génétiquement modifiée ? », Science & Pseudo- Sciences, n° 314, octobre 2015, p. 46-48.
Decreto-Lei n.° 160/2005, Diário da República, I Série-A, n° 182, 21 septembre 2005, p. 5642-5648.
Voir « Selon la recherche européenne, la coexistence entre les produits GM et non GM est possible », inra.fr, 19 mai 2015.
La possibilité de dissémination non intentionnelle des transgènes entre espèces différentes doit être considérée de manière différente selon qu’il s’agit des espèces interfertiles ou d’espèces qui ne peuvent pas s’hybrider entre elles, indique Jean-Claude Pernollet dans le bilan qu’il a dressé en 2018 des risques et avantages environnementaux des plantes biotech. Dans le second cas, souligne- t-il, « l’insertion d’un transgène viable et sa sélection demandent beaucoup de temps de sorte qu’elle n’est pas observable à une échelle de temps humaine34 », tandis que dans le premier cas il faudra prendre des mesures de coexistence des variétés cultivées en observant des distances à respecter entre les parcelles ou en décalant les semis, si on veut éviter à tout prix d’éventuelles hybridations fortuites qui, rappelons-le, n’ont pas de conséquences négatives sanitaires et environnementales.
Ce problème est surtout soulevé par les exploitants qui pratiquent l’agriculture biologique dont le cahier des charges refuse la culture des plantes biotech et l’utilisation de certains pesticides organiques de synthèse (tout en acceptant, cependant, des pesticides chimiques minéraux écotoxiques comme les bouillies à base de cuivre ou des variétés cultivées comme le blé Renan issues de croisements par des méthodes de génie génétique35). Une présence fortuite de plantes GM à une teneur supérieure à 0,9% dans leurs parcelles aurait une incidence économique sur la valeur de leurs récoltes qui ne seraient plus considérées comme « bio ».
Cependant, la coexistence entre les agricultures biotechnologique (GM), conventionnelle et biologique n’est pas impossible. Au Portugal, elle est garantie par le décret-loi 160/200536 qui a établi des règles administratives et des normes techniques. Ces dernières doivent s’appuyer sur les progrès scientifiques et techniques (article 8), et ont conduit à mettre en place des zones géographiques dédiées. La région de Lisbonne et de l’Alantejo possèdent des caractéristiques d’aménagement du territoire (taille et répartition des exploitations agricoles notamment) favorables à la coexistence des différents types d’agricultures (biotechnologique, conventionnelle et biologique).
Le programme européen Practical Implementation of Coexistence in Europe (Price) a livré ses conclusions en 2015 et démontré par des expérimentations réalisées en Espagne que la coexistence entre les cultures GM et les autres est possible37. Il convient d’appliquer des mesures comme l’utilisation de plantes incapables de se reproduire par autopollinisation (mâles stériles), de pratiquer les semis décalés ou l’aménagement de zones tampon. L’application de ces mesures techniques dans les expérimentations a permis d’assurer la conformité des récoltes respectant le seuil d’étiquetage officiel européen de présence fortuite d’OGM de 0,9%.
Prévenir les résistances
Voir « Learn More about Refuge Requirements », monsanto.com, s.d.
Voir Fei Yang, David Kerns et Fangneng Huang, « Refuge-in-the-Bag Strategy for Managing Resistance to Bt Maize », Outlooks on Pest Management, vol. 26, n° 5, octobre 2015, p. 226-228.
Nous nous référons aux évaluations scientifiques unanimes de toutes les agences sanitaires mondiales, à l’exception, et sans entrer dans la polémique politico-judiciaire qui s’ensuivit, de celle du Centre international de recherche sur le cancer (Circ) de 2015, entachée de conflits d’intérêts.
Dès lors qu’un contrôle d’insectes ravageurs est opéré, que ce soit par des méthodes classiques utilisant des formulations phytopharmaceutiques chimiques (minérales ou de synthèse) ou d’origine biologique, ou par un procédé biologique comme la production par une plante biotech d’une protéine toxique pour l’insecte qui s’en nourrit, des phénomènes de résistance sont prévisibles selon les schémas darwiniens de coévolution.
Pour les retarder, il est préconisé de mettre en place des « zones refuges » cultivées en plantes conventionnelles jouxtant les parcelles cultivées avec des plantes transgéniques de manière à opérer un brassage génétique entre les insectes se nourrissant dans les différentes zones, et à diminuer ou à retarder l’apparition de résistances chez l’insecte ciblé. Ces zones refuges ont été fixées à 20% de la superficie de la parcelle cultivée avec une plante biotech intégrant un seul événement de transformation. Plusieurs schémas ont été recommandés : alternance de bandes dans le champ, encerclement ou juxtaposition. La distance maximum entre les plantes transgéniques et conventionnelles ne doit pas excéder 750 mètres. La mise en culture de plantes biotech intégrant
plusieurs éléments de transformation, en multipliant les toxines insecticides, constitue également une réponse pour différer l’apparition de résistances. Le pourcentage consacré aux zones refuges est fixé en fonction de la culture. Ainsi, aux États-Unis, dans les zones de production de coton, l’Environmental Protection Agency (EPA), a fixé un pourcentage de zone refuge de 50% et, pour les cultures GM qui contiennent plusieurs gènes Bt (empilage), une zone refuge de 5%38.
Afin d’alléger le travail des agriculteurs, un nouveau procédé leur est proposé, appelé « Refuge in the bag » (technologie RIB) : le sac de semences contient un mélange déterminé de semences Bt et non-Bt fixé en fonction du pourcentage requis de zones refuge pour la variété transgénique cultivée. L’agriculteur sème en un seul passage les deux types de semences qui sont alors éparpillées dans son champ. Cette technologie présente l’avantage d’inciter et d’obliger l’agriculteur à observer la mise en place d’espaces refuge dans son champ, ce qui n’est pas toujours le cas quand il faut le structurer en zones distinctes. L’exercice peut en effet se révéler très complexe avec les maïs Bt contenant des empilages de gènes, par exemple avec les variétés de maïs Bt Genuity® SmartStax™ qui contiennent six gènes différents (cry1A.105, cry2Ab2, cry1F, cry3Bb1, cry34Ab1, cry35Ab1), ce qui les protège d’insectes ravageurs aériens (lépidoptères) et souterrains (coléoptères). C’est pour cette raison que l’EPA a approuvé en 2010 la technologie RIB. Les modèles mathématiques ont été concluants, mais il semblerait qu’il soit un peu tôt pour dresser un bilan étayé de l’efficacité de cette stratégie39.
Pour lutter contre ces résistances, il faut également observer les bonnes pratiques agricoles (BPA). Ainsi la pratique d’une monoculture ou encore l’usage répété d’un même herbicide d’une culture sur l’autre conduisent inéluctablement à accélérer l’apparition des résistances. Le cas du glyphosate est à cet égard éloquent. Il était déjà utilisé abondamment bien avant la mise sur le marché des plantes biotech, car c’est un herbicide non sélectif parmi les moins toxiques et les plus efficaces40. Le premier cas de résistance à cet herbicide d’une mauvaise herbe, l’ivraie raide (Lolium rigidum), avait été décrit en Australie dès 1996 dans une exploitation agricole conventionnelle. La diffusion des plantes biotech tolérantes au glyphosate (soja et maïs notamment) sur une large échelle et le succès de cet herbicide facile d’emploi après des agriculteurs allaient amplifier des phénomènes d’apparition de résistance chez plusieurs adventices (mauvaises herbes). L’utilisation d’une année sur l’autre de maïs Round-up Ready cultivé en monoculture ou de rotations de cette culture en alternance du soja Round-up Ready (tolérance au même herbicide), comme cela se fait dans certaines régions du continent nord-américain, a conduit à augmenter ce risque de résistance. Il est nécessaire de diversifier les substances actives dans les traitements phytopharmaceutiques : cultiver des plantes biotech ne dispense pas du respect des règles de l’agronomie.
Conclusion
Voir Well Fed, film de Hidde Boersma, Karsten de Vreugd et Philip Fountain qui traite du sujet des plantes biotech et de la culture de l’aubergine Brinjal Bt au Bangladesh (disponible en accès libre sur le lien https://vimeo.com/188913344).
Anthony M. Shelton et al., « Bt Eggplant Project in Bangladesh: History, Present Status, and Future Direction », Frontiers in Bioengineering and Biotechnology, vol. 6, article n° 106, août 2018.
Il apparaît que les plantes biotech se révèlent très utiles à de nombreux égards :
- pour apporter des réponses aux problèmes que posent les bioagresseurs des cultures. Ceux-ci occasionnent une perte économique pour le producteur en détruisant une partie des récoltes ou en les rendant impropres à la vente et ils sont aussi source de problèmes sanitaires, comme les mycotoxines qui, à partir de l’installation de champignons microscopiques pathogènes sur les cultures dans les champs, contaminent les animaux qui consomment ces récoltes, les rendent malades et polluent les aliments destinés à l’homme (céréales, lait, fromage) ;
- pour apporter des réponses au changement climatique avec, d’une part, des variétés adaptées à la sécheresse et, d’autre part, une réduction de l’émission de gaz à effet de serre émis par les engins agricoles ;
- pour diminuer la pénibilité du travail de l’agriculteur par des améliorations techniques et la diminution du nombre de traitements phytosanitaires, avec une conséquence directe sur la santé des petits paysans des pays en développement en zone tropicale. Le recours aux plantes biotech leur évite les conditions rustiques d’épandages de produits phytosanitaires très pénibles et très fréquents, s’accompagnant le plus souvent d’équipements de protection individuelle des plus sommaires. C’est une des clés du succès mentionnée par les petits agriculteurs du Bangladesh qui ont adopté la culture de l’aubergine Brinjal Bt41, l’autre raison étant l’amélioration des rendements, donc un meilleur revenu42.
Les plantes biotech constituent ainsi des outils fondamentaux à prendre en considération pour protéger la santé humaine, animale, végétale et environnementale dans la démarche globale One Health, une seule santé, un seul monde. Les recherches dans ce domaine s’avèrent cruciales pour l’avenir de l’humanité.












