OGM et produits d'édition du génome : enjeux réglementaires et géopolitiques
Introduction
Une situation mondiale contrastée
La forte progression des cultures biotech
Un grand clivage mondial
Une course à l’innovation dans un monde réglementaire hétérogène
Organismes génétiquement édités (OGM) : la course à l’innovation et au dépôt de brevets
Une réglementation européenne qui s’appuie sur le principe de précaution
Conclusion
Résumé
Les méthodes de modification du génome sont intimement liées à l’histoire des hommes, depuis les premiers balbutiements de l’agriculture au néolithique jusqu’au développement des thérapies géniques au cours du XXe siècle. À présent, les techniques employées sont issues des biotechnologies (transgénèse, mutagénèse, ainsi que les nouvelles techniques d’édition du génome regroupées sous le vocable de NBT, pour new breeding techniques) et suscitent un débat sociétal empreint d’inquiétude ou de rejet idéologique.
Ces craintes sont-elles fondées ? En tout cas, les avancées scientifiques que propose cette approche biotechnologique méritent d’être prises en considération, tout particulièrement en matière de santé.
Aujourd’hui, la mondialisation fait que les santés, qu’elles soient humaine et animale, végétale ou environnementale, sont interdépendantes et peuvent être réunies dans le concept One Health : une seule santé, un seul monde.
Dans cette note, nous examinons les enjeux réglementaires, actuels et futurs, concernant les organismes génétiquement modifiés (OGM) et les produits d’édition du génome (OGE), ainsi que l’incidence géopolitique résultant de la défiance qui, dans certains pays, accompagne l’apparition de ces biotechnologies.
Catherine Regnault-Roger,
Professeure des universités, membre de l'Académie d'agriculture de France.
Professeur des universités émérite de l’université de Pau et des Pays de l’Adour (Iprem UMR CNRS 5452 -e2S UPPA), membre de l’Académie d’agriculture de France, membre correspondant de l’Académie nationale de pharmacie, membre du comité scientifique du Haut Conseil des biotechnologies.
Introduction
François Rabelais, Pantagruel, VIII, in Œuvres complètes, Gallimard, « Bibliothèque de la Pléiade », 1994, p. 245.
« Le regard des Français sur l’agriculture. Résultats », étude Ipsos pour Opinion Valley, octobre 2018, p.9. Les organismes génétiquement modifiés (OGM) et les plantes génétiquement modifiées (PGM) seront également appelées ici plantes biotechnologiques ou biotech.
Voir Catherine Regnault-Roger, Des outils de modification du génome au service de la santé humaine et animale et Des plantes biotech au service de la santé du végétal et de l’environnement, Fondation pour l’innovation politique, janvier 2020.
« Science sans conscience n’est que ruine de l’âme », écrivait déjà Rabelais au XVIe siècle1. Ce jugement de Gargantua destiné à l’éducation de son fils Pantagruel est sans doute ce qui représente le mieux l’état de la réflexion sur la controverse sociétale, qui a traversé tout le XXe siècle et qui sévit plus que jamais aujourd’hui, à propos des avancées technologiques et des progrès qu’elles génèrent pour la société. C’est une défiance généralisée qui touche des domaines aussi différents que la physique avec le nucléaire, la chimie avec les pesticides organiques de synthèse ou les matières plastiques dérivées du pétrole, mais aussi la biologie à travers les techniques de modification du génome qui ont pris leur essor au cours du XXe siècle sous la désignation de « biotechnologies ».
L’utilisation de ces biotechnologies pour améliorer la santé du végétal a depuis une quarantaine d’années été au centre d’une polémique sociétale qui cristallise aujourd’hui les débats, à tel point qu’en 2018, 75% de nos concitoyens sont attentifs à ce que leur alimentation ne contienne pas d’organismes
génétiquement modifiés (OGM)2, attitude qui traduit au minimum une suspicion. Sans doute supposent-ils que les OGM sont néfastes pour leur santé, ce qui est loin d’être une réalité étayée sur des faits. Au contraire, les OGM et les organismes génétiquement édités (OGE), issus des nouvelles techniques d’édition génomique (New Breeding Techniques, NBT) se révèlent des outils utiles pour la santé humaine, animale et des plantes cultivées ainsi que pour préserver l’environnement et s’adapter aux changements climatiques3.
Cette défiance envers les OGM a conduit le monde à se diviser en deux parties : d’un côté, les pays qui ont adopté les biotechnologies ; de l’autre, ceux qui les ont rejetées, au moins dans le domaine agricole. Quelle carte du monde en résulte- t-il et quelles sont les perspectives ? Cet examen conduira à se demander quel rôle a joué la réglementation dans la situation actuelle des OGM et la méfiance qu’ils suscitent. Il est important en effet d’en cerner le contexte et les exigences. Depuis l’instauration des premières mesures réglementaires dans le cadre de l’Union européenne, les connaissances scientifiques ont accompli d’importants progrès. Par conséquent, il est aujourd’hui pertinent et légitime de se demander si la réglementation européenne est toujours bien proportionnée aux risques encourus et quels sont les enjeux géopolitiques de la future réglementation qui sera appliquée aux OGE. Autant de questions auxquelles nous allons tenter d’apporter des éléments d’information à partir des réalités scientifiques.
Une situation mondiale contrastée
La forte progression des cultures biotech
Voir Catherine Regnault-Roger, Des plantes biotech…, op. cit.
Voir « Global Status of Commercialized Biotech/GM Crops in 2017: Biotech Crop Adoption Surges as Economic Benefits Accumulate in 22 Years », ISAAA Briefs, n° 53, 2017.
Voir « Global Status of Commercialized Biotech/GM Crops in 2017: Biotech Crops Continue to Help Meet the Challenges of Increased Population and Climate Change », ISAAA Briefs, n° 54, 2018.
Entre 1984 et 1995, de très nombreuses expérimentations (25.000) en champ ont précédé la mise en culture et la commercialisation de plantes génétiquement modifiées (PGM) issues de transgénèse4. Quarante-cinq pays ont hébergé ces essais de terrain, mais près des trois quarts ont été réalisés aux États-Unis et au Canada et les 7.000 autres essais se sont déroulés en Europe, en Amérique du Sud, en Asie et en Afrique du Sud5. À l’issue des procédures d’autorisation, ce sont cinq pays qui se sont lancés en 1996 dans l’aventure de la culture des PGM : les États-Unis, le Canada, l’Argentine, l’Australie et le Mexique, accompagnant ainsi un sixième pays, la Chine, pays pionnier qui, dès le début des années 1990, avait déjà commercialisé du tabac et des tomates transgéniques. En 1996, la superficie des plantes transgéniques couvrait 1,7 million d’hectares, dont 51% se trouvaient aux États-Unis et 39% en Chine. Le Canada et l’Argentine en cultivaient 4% chacun, l’Australie et le Mexique moins de 1%. En 1997, la superficie cultivée de plantes transgéniques était passée à 11 millions d’hectares, soit plus de six fois la superficie de l’année précédente. Dix ans plus tard, en 2007, la surface des cultures biotech s’établissait à 114,3 millions d’hectares, soit un bond de 105,1 millions d’hectares. La progression continue et, en 2018, les dernières données statistiques disponibles donnent le chiffre de 191,7 millions d’hectares6, ce qui représente une progression de plus de 77 millions d’hectares au cours de la dernière décennie.
Mais tous les pays ne cultivent pas des plantes biotech. En fait, le monde est séparé en deux sous-ensembles : les régions qui les cultivent et les autres. On trouve, d’un côté, le continent américain et le continent asiatique ainsi que l’Océanie ; de l’autre, le continent européen (à l’exception de quelques pays, comme l’Espagne et le Portugal), y compris la Fédération de Russie, le Moyen-Orient et de nombreux pays africains.
Un grand clivage mondial
Le continent américain à la pointe du progrès
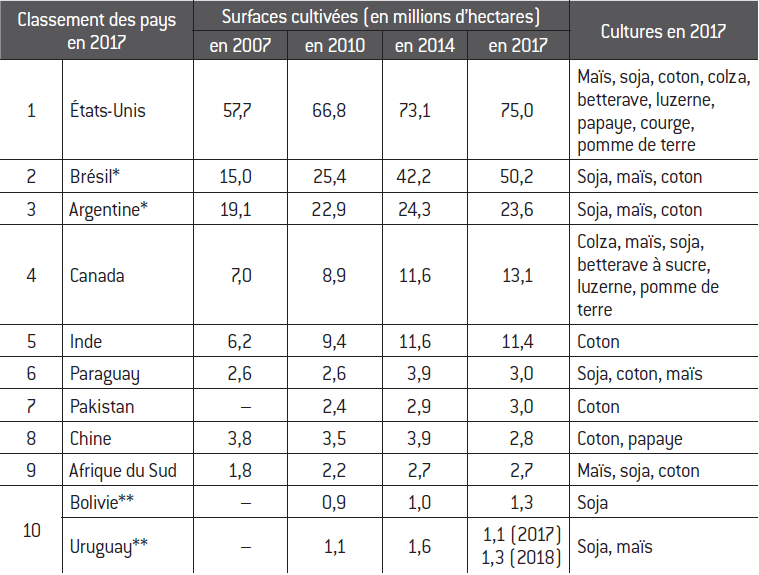
Le continent américain dans son ensemble, nord et sud, représente 87% des terres cultivées en PGM. Les États-Unis sont incontestablement le pays leader avec les plus grandes superficies depuis le début en 1996 jusqu’à aujourd’hui : 75 millions d’hectares cultivés. C’est également le pays qui possède la plus grande diversité de cultures transgéniques commercialisées et le plus grand nombre d’essais. Y sont cultivés du maïs (45% des superficies qui lui sont consacrées en 2017 sont biotech), du soja (45%), des cotonniers (6%), de la luzerne (2%) et du canola-colza (1%), le reste étant plus marginal (betterave à sucre, papaye, courge, pommes Arctic® et pommes de terre Innate®). Depuis 1996, sur vingt ans, les États-Unis ont approuvé 197 événements de transformation dans 19 espèces cultivées dont 43 pour le maïs, 43 également pour la pomme de terre et 25 pour le soja. Ces cultures sont produites par 420.000 fermiers.
Principaux pays producteurs de plantes biotech (2007-2017)
Source :
Source : Fondation pour l’innovation politique ; données issues des différents rapports annuels de l’ISAAA.
* Inversion du classement entre le Brésil et l’Argentine en 2010.
** La Bolivie et l’Uruguay font jeu égal en 2018 avec 1,3 million d’hectares (en raison d’une diminution
des cultures temporaire de 200 000 hectares en Uruguay pour la seule année 2017).
Le canola est du colza génétiquement modifié produit au Voir Canola Council of Canada, « Le canola : les mythes démystifiés », canolacouncil.org, s.d.
Un empilage signifie qu’il y a plusieurs événements de transformation (ici trois) dans une même plante. Voir Catherine Regnault-Roger, Des plantes biotech…, op. cit
Tolérante à un herbicide : HT ; résistante à des insectes : IR.
Voir Catherine Regnault-Roger, Des plantes biotech…, cit.
Voir « Global Status of Commercialized Biotech/GM Crops in 2017… », art. cit.
Vandana Shiva, figure importante de l’activisme écologique et féministe indien et mondial, lutte contre les nouvelles techniques en matière génétique.
Voir Anthony M. Shelton et al., « Bt Eggplant Project in Bangladesh: History, Present Status, and Future Direction », Frontiers in Bioengineering and Biotechnology, vol. 6, article n° 106, août 2018.
Voir Marcel Kuntz, L’Affaire Seralini. Impasse d’une science militante, Fondation pour l’innovation politique, juin 2019.
Gilles-Éric Séralini, Émille Clair, Robin Mesnage, Steeve Gress, Nicolas Defarge, Manuela Malatesta, Didier Hennequin et Joël Spiroux de Vendômois, « RETRACTED: Long term toxicity of a Roundup herbicide and a Roundup-tolerant genetically modified maize », Food and Chemical Toxicology, 50, n° 11, novembre 2012, 4221-4231.
Claudine Franche, « Biotechnologies végétales et pays en développement », in Catherine Regnault-Roger, Louis-Marie Houdebine et Agnès Ricroch (dir.), Au-delà des Science-Innovation-Société, Presses des Mines, 2018, p. 115-134.
Voir Catherine Regnault-Roger, Des outils de modification…, op. cit.
Voir Bernard Le Buanec, Les OGM : Pourquoi la France n’en cultive plus ?, Presses des Mines, 2016.
François Fillon, Faire, Albin Michel, 2015, 137.
Voir Catherine Regnault-Roger, « La réglementation au cœur des débats », in Catherine Regnault-Roger, Louis-Marie Houdebine et Agnès Ricroch (dir.), cit., p. 135-164.
« Loi n° 2014-567 du 2 juin 2014 relative à l’interdiction de la mise en culture des variétés de maïs génétiquement modifié », Journal officiel, 3 juin 2014, p. 9208.
Voir Haut Conseil des biotechnologies (HCB), « Avis en réponse à la saisine du 24 avril 2014 de Messieurs Bernard Accoyer et Jean Bizet suite à la proposition de loi relative à l’interdiction de la mise en culture des variétés de maïs génétiquement modifié sur le territoire français ».
« Directive (UE) 2015/412 du Parlement et du Conseil du 11 mars 2015 modifiant la directive 2001/18/CE en ce qui concerne la possibilité pour les États membres de restreindre ou d’interdire la culture d’organismes génétiquement modifiés (OGM) sur leur territoire », Journal officiel de l’Union européenne, 13 mars 2015, p. L 68/1-68/8.
Catherine Regnault-Roger, « La Réglementation au cœur des débats », art. cit., p. 156.
Le Canada a été le premier pays à autoriser la commercialisation du canola (colza GM7)en 1996. Ce pays arrive aujourd’hui en quatrième position des surfaces cultivées en PGM (12,75 millions d’hectares en 2018) et montre un grand dynamisme de développement. Les principales cultures sont le canola, cultivé sur 67% des surfaces PGM, suivi par le soja (19%) et par le maïs (13,5%). Les cultures de betteraves à sucre (15.000 hectares), de luzerne (4.000 hectares) et de pommes de terre (65 hectares) transgéniques sont plus marginales. Depuis 1996, 177 événements de transformation ont été approuvés par les autorités canadiennes, y compris récemment des triples empilages8 pour le maïs et la pomme de terre. Des aliments provenant de cultures GM, les pommes Artic®, la canne à sucre et le riz doré, ont reçu un agrément pour la consommation.
Les pays d’Amérique latine ne sont pas en reste, et certains comme le Mexique, l’Argentine ou l’Uruguay ont fait partie des pays pionniers qui ont très tôt accueilli des essais entre 1984 et 1995, et les premières cultures en champs en 1996.
En Argentine, avec 18 millions d’hectares, les cultures de soja biotech représentent 75% des 23,9 millions d’hectares GM cultivés, suivies par celles du maïs biotech (5,5 millions d’hectares) et du cotonnier GM, plus marginales (370.000 hectares, en augmentation de 60% entre 2017 et 2018). Ces cultures couvrent plus de la moitié (60%) des terres arables du pays. La totalité du soja cultivé est GM et le taux d’adoption de maïs biotech est de 97%. La majorité des variétés cultivées sont tolérantes à un herbicide9 (83% du soja est HT) ou polyvalentes IR-HT (83% du maïs). On note une forte progression du soja HT-IR Intacta™ qui a été cultivé sur 70.000 hectares en 2015 et sur 3,08 millions d’hectares en 2017. De nouveaux événements de transformation ont été développés par l’Institut de biotechnologies agricoles de Rosario pour une adaptation à la sécheresse et à la salinité, approuvés en 2015, et pour une luzerne GM à faible teneur en lignine qui permet d’augmenter la digestibilité des aliments pour les animaux en 2018 (troisième autorisation mondiale accordée, après celles des États-Unis et du Canada).
Le Brésil a démarré les cultures GM en 2003, plus tardivement que l’Argentine, mais l’a supplantée depuis avec une superficie de 51,3 millions d’hectares consacrée aux cultures biotech (plus de la moitié des terres arables) ; en 2018, il se classe juste derrière les États-Unis. Le soja occupe les deux tiers des superficies cultivées biotech (34,86 millions d’hectares), le dernier tiers se partage entre le maïs (15,38 millions d’hectares) et le coton (1 million d’hectares). La part de plantes transgéniques est très élevée dans ces trois cultures : 97% pour le soja, 89% pour le maïs et 84% pour le cotonnier. Elles sont majoritairement HT, mais les empilages de gènes se développent (75% de maïs et 59% de cotonnier cultivés en 2017 sont IR-HT). La canne à sucre GM a fait son apparition en 2018 sur 400 hectares. Parmi les 68 événements de transformation qui ont été approuvés dans ce pays figurent aujourd’hui plusieurs empilages qui confèrent au soja une double tolérance à deux herbicides différents (glufosinate et dicamba) ou encore, accompagnant deux gènes de résistance à des insectes, une triple tolérance à trois herbicides différents (glyphosate, glufosinate et 2-4D), ce qui permet de varier les traitements herbicides et, par conséquent, retarde l’apparition des résistances chez les adventices10.On observe que 80% des exportations de soja brésilien vont en Chine.
Le Paraguay et l’Uruguay, deux autres pays du Mercosur, sont petits par la taille mais majeurs en termes de cultures agricoles biotechnologiques. Ils figurent tous les deux dans le top 10 des pays cultivant des plantes biotech.
Au Paraguay, le soja HT tolérant au glyphosate (Roundup Ready®), autorisé dès 2004, est la culture GM dominante et occupe 91% des surfaces biotech cultivées, loin devant le maïs (9%) et le cotonnier (marginal). Ces cultures, qui concernent 10.000 exploitations agricoles, occupent 62% des terres arables du pays. Le soja paraguayen est à 96% transgénique, avec un développement au cours des dernières années d’empilages HT-IR qui sont passés de 17% en 2016 à 35% en 2017. Quant au maïs, en 2017, il était polyvalent IR-HT à 83%.
En Uruguay, ce sont 3.000 exploitations agricoles qui développent du soja et du maïs biotech. Le soja représente la presque totalité des surfaces biotech cultivées (1,09 million d’hectares). On constate que les 50.000 hectares de maïs cultivés présentent un taux d’adoption de 100%, c’est-à-dire que la totalité des cultures uruguayennes de maïs en 2017 étaient biotechnologiques (taux d’adoption de 85,7% en 2016). En 2017, on a observé une diminution des cultures GM en Uruguay (– 13%), comme dans d’autres pays du Mercosur (– 16% au Paraguay, – 3% en Argentine). Selon l’International Service for the Acquisition of Agri-biotech Applications (ISAAA), cette réduction serait liée aux bas prix des récoltes et aux fluctuations du commerce international ainsi qu’à des aléas climatiques marqués, à des inondations mais surtout une sécheresse sévère qui ont affecté plusieurs pays d’Amérique latine cette année-là.
Au-delà des sojas, maïs et cotonniers biotech, les autres pays d’Amérique latine (Bolivie, Mexique, Colombie, Honduras, Chili et Costa Rica) développent, sur de petites surfaces, des cultures de lin, de riz, d’ananas et aussi d’œillets bleus pour l’exportation (Colombie). Entre 2016 et 201711, les cultures GM ont progressé significativement dans plusieurs pays : au Chili (+ 23%), au Costa Rica (+ 22%), au Mexique (+ 13%) et en Colombie (+ 7%).
On note que le continent américain, dans son ensemble, est celui qui a, et de loin, le plus adhéré à la culture des plantes biotech.
Le développement remarqué du continent asiatique et de la zone Pacifique
La Chine a été le premier pays à commercialiser des plantes transgéniques au début des années 1990, avec du tabac et des tomates résistants à des virus, puis, en 1997, des cotonniers Bt (IR) pour lutter contre des lépidoptères nuisibles, ainsi que des papayes GM, résistantes au Papaya ringspot virus (PRSV) et cultivées sur une petite surface pour l’alimentation humaine. En 2017, la culture des papayes GM occupait 7 130 hectares, avec un taux d’adoption de la culture transgénique de 86%, et le cotonnier IR, 2,8 millions d’hectares, avec un taux d’adoption de cotonnier transgénique de 95%, soit la presque totalité des surfaces cultivées en cotonnier. Ce sont 7 millions d’agriculteurs qui sont concernés par ces deux cultures. La Chine a également approuvé 64 événements transgéniques pour des importations ou des mises en cultures de cotonnier, colza (canola argentin), maïs, papaye, pétunia, peuplier, riz, soja, betterave à sucre, poivron et tomate. La politique volontariste des autorités chinoises pour promouvoir les biotechnologies s’est concrétisée par un financement de 3 milliards de dollars accordés aux instituts de recherche et sociétés chinoises pour développer des lignées biotechnologiques de blé et de maïs résistants à la sécheresse, de riz résistant aux maladies, de soja avec un profil d’huile amélioré et des rendements accrus.
L’Inde, elle, a développé des plantations de cotonniers génétiquement modifiés pour résister à des insectes dès 2002, mais c’est à partir de 2007 que ces cultures ont été majoritaires, avec un taux d’adoption de 60%, qui atteint 93% en 2017. Avec une superficie de 11,6 millions d’hectares en 2018, l’Inde est aujourd’hui le pays asiatique qui a les plus grandes surfaces de cultures biotech. Cependant, la situation des plantes transgéniques sur l’ensemble du territoire indien est complexe. En effet, ce pays est composé d’États qui n’ont pas tous adopté la même position envers les OGM et qui doivent faire face à un lobbying de mouvements anti-OGM puissants dont Vandana Shiva12 est la figure de proue. Des essais expérimentaux pour diversifier les cultures ont cependant été réalisés avec plusieurs espèces : pois chiche, moutarde, riz, canne à sucre et aubergine. Dans le cadre de partenariats avec plusieurs pays de l’Asie du Sud et du Sud-Est (Bangladesh, Indonésie, Philippines) se développent plusieurs programmes de recherche et d’essais en champs de papayes à mûrissement retardé, de cotonniers résistants à des insectes ou de riz nutritionnellement amélioré. Le Pakistan, pays voisin, cultive 2,8 millions d’hectares de diverses variétés de cotonnier IR (34 ont été approuvées entre 2010 et 2016) et développe également des essais de maïs HT ou empilés IR-HT.
Six pays du Sud et du Sud-Est asiatique et de la zone Pacifique développent également de petites surfaces de cultures transgéniques sur moins de 1 million d’hectares : les Philippines cultivent 630.000 hectares de maïs ; le Myanmar, 310.000 hectares de cotonnier ; le Vietnam, 49.000 hectares de maïs ; l’Australie, 793.000 hectares de cotonnier et de canola ; et le Bangladesh, 2.975 hectares d’aubergine. En 2018, l’Indonésie a débuté la culture de la canne à sucre tolérante à la sécheresse sur 1.342 hectares.
Les tribulations de la culture de l’aubergine méritent qu’on s’y attarde. En effet, l’aubergine (appelée aussi brinjal) est originaire d’Inde, qui en produit plus de 13,5 millions de tonnes par an, soit 25% de la production mondiale. Se rangeant juste derrière la Chine, l’Inde est le deuxième producteur d’aubergine du monde. Cette culture largement répandue est ravagée par un lépidoptère qui provoque des pertes de récolte allant de la moitié aux trois quarts. Pour limiter ces dégâts, des traitements insecticides répétés et rapprochés (20 à 40 traitements par saison en Inde) sont effectués, avec des moyens souvent rudimentaires qui ne sont pas sans conséquence pour la santé des agriculteurs et pour l’environnement. Ce légume apporte dans l’alimentation des populations peu favorisées du sous-continent indien des compléments importants (vitamines, minéraux, fibres et antioxydants). Pour trouver une solution aux ravages de l’insecte, la société Mahyco, premier producteur de semences en Inde (mais dont Monsanto détenait à l’époque 26% du capital), a développé, en collaboration avec l’université de Tamil Nadu, des variétés locales d’aubergines Bt résistantes aux lépidoptères ravageurs. Malgré des essais concluants en champs réalisés entre 2002 et 2006, les autorités indiennes n’ont pas accordé l’autorisation de la commercialiser sous la pression des ONG anti-OGM. Le moratoire indien de 2010 s’est accompagné en 2011 d’un arrêt, pour les mêmes raisons, des essais réalisés aux Philippines où l’aubergine est pourtant le légume le plus cultivé. De fait, cette innovation pleine de promesses a été enterrée. Cependant, un rebondissement est survenu au Bangladesh, l’un des pays les plus pauvres au monde, dans lequel l’aubergine est la troisième culture agricole. En 2014, avec le soutien du ministère de l’Agriculture, des essais sur champs ont été réalisés avec les variétés d’aubergines Bt développées en Inde : 20 agriculteurs en ont débuté la culture sur 2 hectares, avec des rendements augmentés de 30% et une réduction de 30 à 70% des traitements insecticides. En dépit des intimidations appuyées d’ONG anti-biotechnologies envers les producteurs, les surfaces de culture commerciale de brinjal Bt ont continué à progresser pour couvrir, en 2017, 2.400 hectares exploités par 27.000 agriculteurs et, en 2018, près de 3.000 hectares. Une étude récente a comparé 505 exploitations cultivant l’aubergine transgénique à 350 exploitations produisant des variétés conventionnelles : à une économie de pesticides de 61%13, s’ajoute pour les agriculteurs producteurs de brinjal Bt, une multiplication par six du revenu à l’hectare. Le Bangladesh mène actuellement une politique très volontaire d’adoption de cette culture alimentaire biotech.
Le continent africain : entre doutes et aspirations
Si de nombreux essais sont en cours en Afrique de l’Ouest – Burkina Faso, Cameroun, Ghana et Nigeria – et en Afrique de l’Est – Kenya, Mozambique, Malawi, Ouganda – avec, entre autres, des cultures de niébé, de maïs, de sorgho, de coton, de patate douce, de riz, de banane et de soja, seuls deux pays cultivent actuellement des plantes biotech : le Soudan, avec 243.000 hectares de cotonnier IR, et l’Afrique du Sud, sur 2,7 millions d’hectares (voir tableau page 12). Un troisième pays de ce continent vient tout juste de les rejoindre : l’Eswatini (ex-Swaziland), avec 250 hectares de cotonnier IR plantés en 2018.
Plusieurs essais de cultures transgéniques ont été conduits dans certains pays, comme au Burkina Faso (cotonnier IR) ou encore au Kenya (projet de cotonnier tolérant à un herbicide) puis abandonnées :
– au Burkina Faso, certaines variétés intégrant l’événement transgénique Bt afin de lutter contre le ver du cotonnier présentaient le défaut de produire des fibres de coton plus courtes que les variétés conventionnelles. Malgré la réduction des traitements de pesticides et l’augmentation des rendements, la commercialisation de la récolte de ce coton était moins lucrative et les paysans burkinabés ont abandonné ces variétés qui ne correspondaient pas à leurs espérances ;
– au Kenya, l’affaire Séralini14, avec la publication de photos de rats déformés par des tumeurs à la une des journaux, a marqué les esprits, même si depuis, l’article de recherche incriminé15 a été invalidé par la communauté scientifique et rétracté par la revue qui l’avait publié.
Pour expliquer les hésitations africaines, Claudine Franche, de l’Institut de recherche pour le développement (IRD), évoque « de multiples facteurs parmi lesquels on peut citer l’absence de volonté politique pour la mise en place de l’encadrement législatif et juridique nécessaire, le risque de voir le secteur agricole sous l’emprise de grandes multinationales, le manque d’expertise scientifique permettant une analyse bénéfices-risques approfondie de ces cultures, et enfin l’influence, sur ce continent, de l’Europe où le principe de précaution prévaut16».
Un projet international cependant attire l’attention : le projet Water Efficient Maize for Africa (WEMA) en vue d’adapter la culture du maïs à la sécheresse. Il résulte d’un partenariat public-privé entre le Centro internacional de mejoramiento de maíz y trigo (CIMMYT, « Centre international d’amélioration du maïs et du blé ») qui fournit des variétés de maïs à haut rendement adaptées aux conditions africaines, et des organismes nationaux de recherche agricole installés au Kenya, au Mozambique, en Ouganda, en Afrique du Sud et en Tanzanie qui fournissent les infrastructures de mise au point, et également la société Monsanto (aujourd’hui Bayer) qui apporte sa connaissance de l’événement transgénique MON 87460 intégré dans des variétés de maïs.
Cultivées pour la première fois aux États-Unis en 2013 et en Afrique du Sud en 2014, les variétés de ce maïs transgénique ont des rendements supérieurs de 7 à 15% en conditions de stress hydrique. Les tests pour mettre au point des empilages de gènes (IR, meilleure utilisation de l’azote) se poursuivent dans les pays africains partenaires de ce projet. Financé par la Fondation Bill et Melinda Gates et la Fondation Howard G. Buffett ainsi que par l’United States Agency for International Development (USAID), le projet WEMA devrait mettre des semences libres de droit à la disposition des agriculteurs africains.
Le continent européen se distingue par son hostilité aux biotechs
Le continent européen est dans sa grande majorité très hostile à la culture des plantes transgéniques. Seuls deux pays de l’Union européenne, l’Espagne et le Portugal, résistent encore, dans un environnement communautaire peu encourageant. Mais on rappellera que si l’Union européenne ne cultive que très marginalement les plantes biotech, elle en importe massivement : c’est, derrière la Chine, le deuxième importateur mondial de soja, dont la culture est à 80% transgénique.
En Europe, en 2018, la péninsule Ibérique a hébergé des champs de maïs MON 810, à savoir la seule plante transgénique cultivée dans l’Union européenne, sur une superficie de 120.990 hectares. On note cependant une diminution de la culture qui atteignait 131.535 hectares (124.227 hectares en Espagne, 7.308 hectares au Portugal) en 2017. Il existe une pression psychologique très forte dans l’Union européenne à l’encontre des cultures GM, et les importations de maïs en Espagne en provenance d’Amérique du Sud et des États-Unis (majoritairement GM) exercent une concurrence très vive.
Le maïs MON 810 est un maïs Bt (IR) cultivé depuis plus de quinze ans en Espagne sans incident et au grand bénéfice des agriculteurs qui le plantent. Ils économisent des traitements d’insecticides et leurs récoltes contiennent moins de mycotoxines. En effet, ce sont dans les régions où la pyrale du maïs et la sésamie, deux insectes ravageurs majeurs de la culture, sont endémiques et exercent une forte pression parasitaire, telles qu’en Aragon, en Catalogne et, dans une moindre mesure, en Estrémadure, que se concentrent les surfaces cultivées en MON 810 (82% de la superficie totale). D’une année sur l’autre, l’agriculteur choisit de cultiver du maïs transgénique ou de revenir aux variétés conventionnelles si la pression parasitaire a temporairement diminué, comme cela a été le cas en Catalogne dans les années 2010. Au Portugal, le MON 810 est cultivé dans l’Alentejo et dans la région de Lisbonne où la taille des exploitations agricoles, suffisamment importantes, n’est pas un obstacle à la réglementation européenne sur la coexistence des agricultures17.
Auparavant, le MON 810 était cultivé aussi en République tchèque et en Slovaquie pour alimenter le bétail ou la filière de biocarburant, mais des campagnes anti-OGM ont entravé ce développement. Il a existé aussi des cultures pommes de terre transgéniques Amflora, dont l’amidon présentait des propriétés intéressantes pour la biodégradabilité de composés industriels (emballage, adhésifs, textile, etc.) et les produits de la féculerie, réalisées en Allemagne, en Suède et en République tchèque. Autorisées en 2010 par la Commission européenne, ces cultures furent abandonnées deux ans plus tard à la suite de saccages de parcelles par des activistes. La société BASF, qui commercialisait cette pomme de terre, a alors décidé de délocaliser cette activité aux États-Unis en 2012. Depuis, plusieurs sociétés françaises et étrangères ont suivi cet exemple et ont déplacé leurs activités de recherche et développement sur les biotechnologies vers le continent américain (nord et sud).
Aujourd’hui, après l’avoir acceptée un temps, la plupart des pays de l’Union européenne rejettent la culture des plantes biotech. Ce rejet est dû à diverses raisons liées aux différents contextes nationaux mais surtout à l’action sans relâche d’ONG anti-OGM comme Greenpeace.
En France, s’agissant des biotechnologies, cela a été une longue suite de renoncements dont Bernard Le Buanec, membre de l’Académie d’agriculture de France et de l’Académie des Technologies, s’est fait l’écho18. Il y détaille une convergence d’attitudes qui cimente ce rejet : celle de la grande distribution, qui met en avant des stratégies de marketing fondées sur l’étiquetage sans OGM (groupe Carrefour) ; celle de la recherche publique des années 1980 (l’Inra et son directeur général Guy Paillotin), qui pratique l’ambiguïté ; celle des syndicats agricoles, qui se montrent plutôt réservés, quand ils ne manifestent pas un rejet franc (Confédération paysanne) ; sans oublier l’attitude de certains médias qui se livrent à une désinformation récurrente. À cela s’ajoutent des destructions régulières d’essais expérimentaux de coopératives, d’organismes officiels d’évaluation des variétés ou d’instituts de recherche, ainsi que des saccages de parcelles cultivées d’exploitants agricoles (quand la culture de maïs GM était autorisée en France, avant 2014) par des activistes environnementalistes et anti-biotechnologies, parmi lesquelles s’illustrent particulièrement Les Faucheurs volontaires, la Confédération paysanne et Greenpeace. La destruction de ces biens privés bénéficie le plus souvent d’une grande mansuétude judiciaire, bien qu’il y ait atteinte au droit de propriété ainsi qu’au bien commun que représente l’expérimentation scientifique.
À partir de 2008, on a également pu noter un changement d’attitude des différents gouvernements français qui sont devenus hostiles à la culture des plantes biotech sur le territoire national. Ce revirement est lié à une sorte de « deal » passé entre le président Nicolas Sarkozy et les Verts, lors du Grenelle de l’environnement de 2007, ainsi que le relate, par exemple, François Fillon, alors Premier ministre : « Il [Nicolas Sarkozy] a arbitré pour l’interdiction totale des OGM et des expérimentations en plein champ […], leur abandon permettait d’obtenir un deal avec les écologistes qui, si on leur accordait cela, ne feraient pas d’obstruction sur la question du nucléaire19.» Les majorités présidentielles qui suivirent furent également à l’écoute de l’écologie politique et s’appuyèrent sur ce « deal » contre les OGM, devenu un pacte appelé à perdurer.
S’ensuivit pendant les six années suivantes un imbroglio politico-réglementaire et ce que j’ai appelé des « pantalonnades scientifiques » car, jusqu’en 2015, la réglementation européenne ne permettait pas d’interdire sur un territoire national la culture de plantes transgéniques autorisées communautairement sauf à évoquer une clause de sauvegarde pour des motifs de mise en péril de la santé ou de l’environnement, ce que les différents gouvernements des présidences Sarkozy et Hollande n’ont pas hésité à faire en produisant des argumentaires scientifiques tendancieux et farfelus, devenant la risée des comités d’experts européens et discréditant chaque fois un peu plus les paroles des scientifiques et des politiques – le Haut Conseil des biotechnologies (HCB) a ainsi été tenu soigneusement à l’écart de ces manœuvres car son comité scientifique était jugé peu malléable pour pratiquer ces dévoiements scientifiques20. L’Autorité européenne de sécurité des aliments (European Food Safety Authority, EFSA), en charge de l’examen du bien-fondé des demandes françaises, les a rejetées par quatre fois, en 2009, 2011, 2012 et 2014. En conséquence, la Cour de justice de l’Union européenne (CJUE), suivant des avis de l’EFSA, a annulé les moratoires imposés par les gouvernements français successifs, ce qu’a ensuite entériné le Conseil d’État français.
Le point d’orgue de cette farce politico-scientifique fut la publication, le 2 juin 2014, d’une « petite loi » qui interdisait la mise en culture des variétés de maïs génétiquement modifié sur le territoire français21 (à partir d’un argumentaire scientifique infondé, comme cela fut démontré par le HCB22), puis l’adoption d’une directive modifiant la réglementation européenne et autorisant un État membre de l’Union européenne à interdire la culture des OGM pour « des motifs sérieux tels que ceux liés à des objectifs de politique environnementale ; à l’aménagement du territoire ; à l’affectation des sols ; aux incidences socio- économiques ; à la volonté d’éviter la présence d’OGM dans d’autres produits […] ; à des objectifs de politique agricole ; à l’ordre public, ce dernier point devant être évoqué conjointement avec un autre motif23». Les gouvernements français de l’époque ont ainsi pu s’opposer, en toute légalité européenne, à toute culture de plantes génétiquement modifiées sur le territoire national. Ce qu’ils ne manquèrent pas de faire, mettant fin au feuilleton de la culture du maïs Bt MON 810, tour à tour autorisée puis interdite en France. Comme j’ai eu l’occasion de le souligner, on retiendra de cet épisode « que la culture des plantes génétiquement modifiées est interdite en France pour des considérations d’alliances politiciennes, et que la Commission européenne a accepté qu’une réglementation ne repose plus sur les seuls critères scientifiques mais sur les positions politiques et idéologiques des gouvernants de chaque État membre, laissant ainsi le champ ouvert à la subjectivité et à l’arbitraire24».
Une course à l’innovation dans un monde réglementaire hétérogène
Organismes génétiquement édités (OGM) : la course à l’innovation et au dépôt de brevets
Voir Dominik Modrzejewski et al., « What is the available evidence for the range of applications of genome editing as a new tool for plant trait modification and the potential occurrence of associated off target effects: a systematic map », Environmental Evidence, vol. 8, article n° 27, juillet 2019.
Voir Catherine Regnault-Roger, Des outils de modification…, op. cit.
Voir Jacqueline Martin-Laffon, Marcel Kuntz et Agnès Ricroch, « Worldwide CRISPR patent landscape shows strong geographical biases », Nature Biotechnology, vol. 37, n° 6, juin 2019, p. 613-621.
C’est dans le contexte d’un monde divisé sur l’utilité des biotechnologies, entre pays qui les favorisent et ceux qui les interdisent ou en empêchent le développement, qu’intervient aujourd’hui une nouvelle course à l’innovation et au dépôt de brevets pour les produits issus des nouvelles techniques d’édition du génome, les OGE.
Les chiffres sont déjà éloquents. Grâce à deux publications récentes, il est possible de comparer le dynamisme des publications de recherche portant sur les NPBT par pays25 et de regarder en miroir les brevets sur la technologie Clustered Regulatory Interspaced Short Palindromic Repeats (CRISPR)26 qui ont été déposés au cours des six dernières années27.
Répartition géographique des publications de recherches sur les NPBT et des brevets sur la technique CRISPR entre 1996 et 2018.
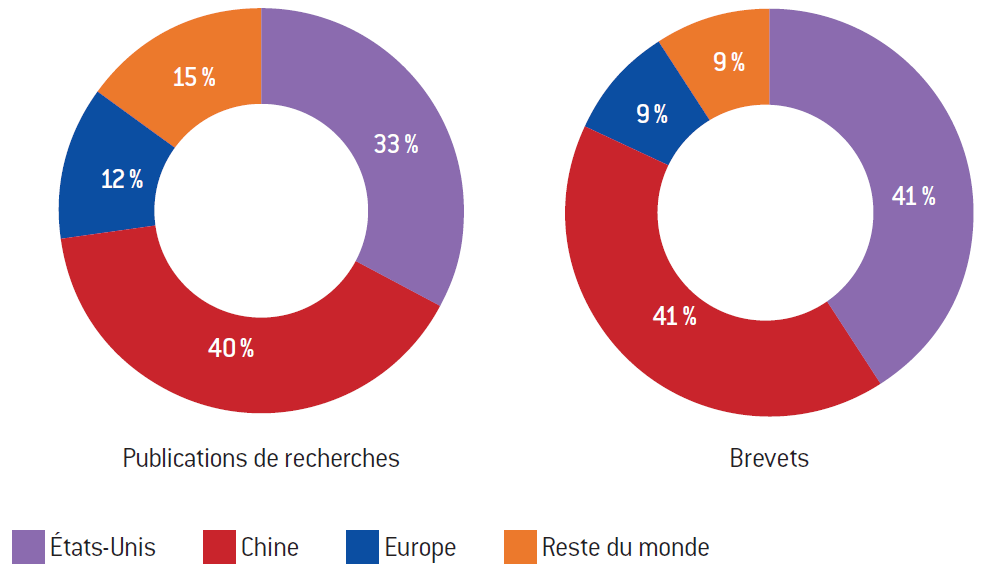
Les travaux de recherche recensés de 1996 à mai 2018 démontrent le dynamisme des laboratoires chinois et américains dans ce nouveau secteur et l’examen des dépôts de brevets sur la période 2012-2018 conforte cette conclusion. Les deux pays les plus inventifs sont sans conteste la Chine et les États-Unis, tant en termes d’amélioration des techniques qu’en termes d’applications. Mais si les laboratoires américains restent des chefs de file en matière d’améliorations techniques et dans le secteur des applications médicales, la Chine a déposé le plus de brevets dans les secteurs des applications industrielles et agricoles (végétales et animales). Les applications dans le secteur des plantes représentent 13% du total des brevets répertoriés.
Répartition géographique et secteurs des applications des brevets CRISPR déposés entre 2012 et 2018
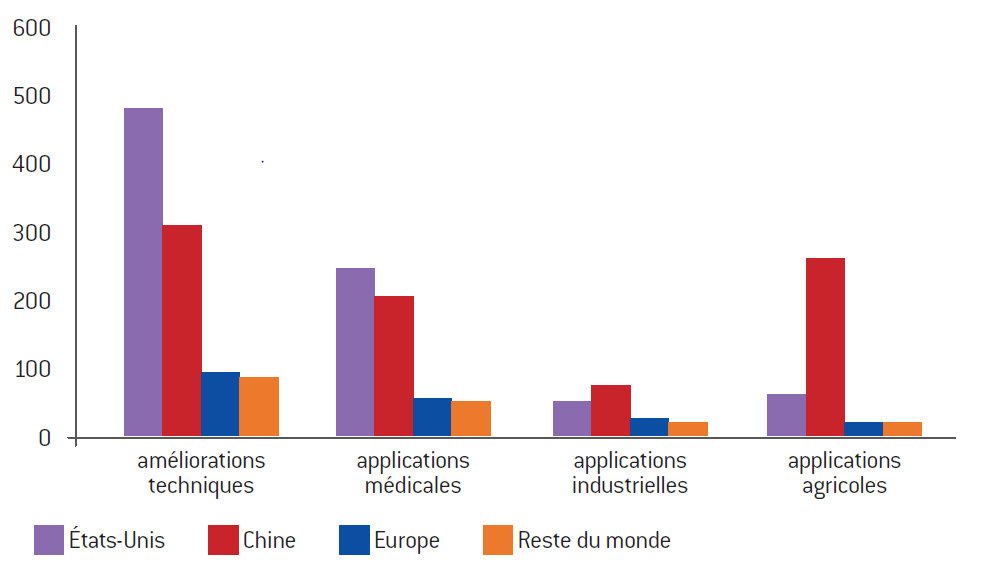
Source :
d’après Jacqueline Martin-Laffon, Marcel Kuntz et Agnès E. Ricroch, « Worldwide CRISPR patent
landscape shows strong geographical biases », Nature Biotechnology, vol. 37, n° 6, juin 2019, p. 613-621.
Voir Arnd Hoeveler et Étienne Magnien, « Quand les instances européennes mènent le bal », Biofutur, n° 172, novembre 1997, 12-15.
Voir Jean Claude Pernollet, « Plantes génétiquement modifiées », in Catherine Regnault-Roger (dir.), Idées reçues et agriculture. Parole à la science, Presses des Mines, 2018, p. 188-204.
On peut constater que l’Europe ne suit pas le mouvement. Avec 9% des brevets déposés et 13% des publications de recherche, elle se situe au même niveau que tous les autres pays du monde réunis (Australie, Japon et pays de l’Amérique latine, l’Afrique étant pour sa part très marginale), très loin derrière les deux chefs de file. Elle prend un retard technologique important, ce qui aura forcément dans le futur une incidence économique et géopolitique.
Pourtant, entre 1989 et 1994, le continent européen dominait l’innovation en matière de biotechnologies et les sociétés européennes avaient déposé plus de brevets sur les biotechnologies que les sociétés américaines (203 contre 178), comme le soulignaient alors deux hauts fonctionnaires de la Commission européenne28.
Ce retard européen dans la production scientifique qu’accompagne une véritable déroute en matière de propriété intellectuelle va probablement s’accentuer au cours des prochaines années si les attitudes réglementaires des pays restent identiques à ce que l’on connaît aujourd’hui, avec certains favorables au développement des biotechnologies et d’autres qui y sont défavorables, ce qui aura des conséquences graves pour leur agriculture. Jean-Claude Pernollet, membre de l’Académie d’agriculture, souligne ainsi que « le blocage pérenne du débat sur les PGM est particulièrement néfaste à l’avenir agricole des pays qui en refusent la culture29». La réglementation, non seulement pour les OGM mais aussi celle qui sera appliquée aux OGE, s’inscrit aujourd’hui dans un véritable enjeu géopolitique.
Une réglementation européenne qui s’appuie sur le principe de précaution
Voir Claudine Franche, « Biotechnologies végétales et pays en développement », art. cit.
Directive 89/219/CEE, 7 mars 1989, et Directive 90/220/CEE, du 23 avril 1990.
Directive 2001/18/CE, 12 mars 2001.
Directive 2015/412, 11 mars 2015.
Directive 2018/350, 8 mars 2018.
Règlement 2015/2283, 25 novembre 2015.
Éléments du contexte réglementaire
À travers le monde, les réglementations auxquelles sont soumises les plantes transgéniques ne sont pas homogènes. Deux logiques s’affrontent : d’un côté, le Bangladesh, la Colombie, le Costa Rica, le Honduras, l’Inde, le Mexique, les Philippines, le Soudan et l’Uruguay fondent leur réglementation, comme le Canada et les États-Unis, sur la nature des produits obtenus ; de l’autre, l’Afrique du Sud, l’Australie, la Bolivie, le Burkina Faso, la Chine, l’Inde et le Pakistan se déterminent, comme l’Union européenne et la Nouvelle-Zélande, à partir des techniques utilisées pour produire les plantes biotech30. Cette différence d’attitude réglementaire n’est pas sans incidence sur l’appréciation des risques liés aux OGM et sur la gestion des autorisations de commercialisation accordées par les pays.
Classiquement, la réglementation dans le domaine de la santé publique et environnementale est destinée à protéger les personnes ou leur environnement d’effets nocifs sur leur santé. Elle prévoit et prend des dispositions en s’appuyant sur des évaluations tangibles et fiables pour gérer les risques, c’est-à-dire limiter l’exposition à ce danger s’il existe, ce qui nécessite de définir ce que serait le danger pris en considération et son occurrence (directement liée à l’exposition des personnes à protéger) afin d’en apprécier pleinement le risque réel.
À la fin du XXe siècle, la transgénèse, alors la plus récente technique de modification du génome, a ouvert l’exploration de nouveaux champs de la connaissance et d’immenses possibilités d’applications. Aussi, devant ces perspectives encore mal cernées, c’est très tôt que la communauté scientifique s’est posé la question d’évaluer quels risques pouvaient être associés à cette nouvelle technologie. Organisé par Paul Berg, biochimiste à l’université de Stanford et futur prix Nobel de chimie en 1980, un débat scientifique fut organisé en 1975, lors d’une conférence réunissant 150 spécialistes à Asilomar en Californie, à la suite duquel furent mises en place des réglementations sur les OGM dans divers pays. Aux États-Unis fut publié en 1986 le Coordinated Framework for Regulation of Biotechnology. En France, la même année, était créée la Commission de génie biomoléculaire (CGB), chargée d’analyser d’éventuels risques potentiels pour la santé et l’environnement liés à l’expérimentation d’OGM en milieu ouvert. Suivit après cela la mise en place d’une réglementation européenne sur les OGM qui intervint en plusieurs étapes : tout d’abord, un jeu de deux directives articulées ensemble et publiées en 1989 et 1990, relatives à l’utilisation d’OGM en milieu confiné ou en milieu ouvert31, puis, dix ans plus tard, en 2001, une directive « relative à la dissémination volontaire d’OGM dans l’environnement32», toujours en vigueur mais amendée en 201533, et enfin, en 2018 une directive réactualisant le cadre réglementaire des dispositions en matière de surveillance de l’évaluation des risques pour l’environnement34. En 2015, un nouveau règlement sur les nouveaux aliments a également été publié pour accompagner ces directives35.
S’appuyant sur le principe de précaution, ce corpus réglementaire de l’Union européenne est de plus en plus exigeant et restrictif pour l’utilisation des OGM (cultures ou importations) dans l’espace européen et il n’est pas étranger à la situation actuelle européenne où une majorité d’États membres se défient de cette technologie et de nombreux refus d’autorisation s’appuient aujourd’hui sur la mention « une opinion négative du public ».
Principe de précaution et réglementation

Molécule d’acide désoxyribonucléique créée en laboratoire par génie génétique.
Christine Noiville et Estelle Brosset, « Les nouvelles techniques d’édition du génome donnent-elles naissance à des OGM couverts par la directive 2001/18 : la Cour de justice de l’Union dit deux fois oui ! », Cahiers Droit, Sciences & Technologies, n° 8, 2018, §17.
Ibid., §19. La question préjudicielle est une question posée par un juge national lorsque la résolution d’un litige qui lui est soumis est conditionnée par l’interprétation d’une norme du droit de l’Union européenne.
Cité in Jean-Baptiste Jacquin, « Tensions entre le Conseil d’État et la Cour de justice de Luxembourg », Le Monde, 17 mai 2019.
Directive 2001/18/CE, op. cit.
Pour plus d’information sur ce faux débat entre l’artificiel et le naturel, voir Catherine Regnault-Roger, Des outils de modification…, op. cit.
Pour plus d’information sur la transgénèse, voir ibid.
Voir EFSA, « Guidance on the Post-Market Environmental Monitoring (PMEM) of genetically modified plants », EFSA Journal, vol. 9, n° 8, août 2011, p. 2316-2247.
Voir Catherine Regnault-Roger, Des plantes biotech…, op. cit.
Groupe d’étude des variétés et des semences (Geves), « Le Catalogue officiel des espèces et variétés de plantes cultivées en France ».
Voir Commission européenne, « Plant variety catalogues, databases & information systems », ec.europa.eu.
Voir Jéremy Rifkin, Le siècle biotech, édition en français, La Découverte, 1998.
Commission européenne, « Group of Chief Scientific Advisors », ec.europa.eu.
« Une perspective scientifique sur le statut réglementaire des produits dérivés de l’édition génomique et ses implications pour la directive OGM », déclaration du groupe des Conseillers scientifiques en chef de la Commission européenne, 13 novembre 2018.
United States Department of Agriculture (USDA), « USDA Proposes New SECURE Biotechnology Regulations to Protect Plant Health and Promote Agricultural Innovation », usda.gov, 6 juin 2019.
Voir « L’Australie et le Japon définissent les règles pour les nouvelles techniques génétiques (NBT) », seppi.over-blog.com, 19 mai 2019.
Voir Claudine Franche, « Biotechnologies végétales et pays en développement », art. cit.
À ce sujet, voir Eddy Fougier, Contester les technosciences : leurs raisons, Fondation pour l’innovation politique, juillet 2011 et Sylvain Boulouque, Contester les technosciences : leurs réseaux, Fondation pour l’innovation politique, juillet 2011.
Voir Hervé Kempf, La Guerre secrète des OGM, Seuil, 2003.
Voir Bernard Le Buanec, op. cit.
Marcel Kuntz, OGM, la question politique, PUG, 2014, 17.
Cité in Bernard Le Buanec, op. cit.
Les Amis de la Terre, « HCB, les Amis de la Terre prennent leurs responsabilités ! », 2016.
À ce tableau général s’ajoute une dernière péripétie juridique liée à l’arrêt du 25 juillet 2018 de la Cour de justice européenne (CJUE) statuant que les produits obtenus par des techniques de mutagenèse postérieures à la directive 2001/18/CE (mutagenèse ciblée) doivent être soumis à la réglementation des OGM, alors que ceux issus des techniques de mutagenèse « traditionnelles » (entendre « utilisées avant 2001 ») peuvent continuer à en être exemptés, une latitude étant cependant accordée aux États membres pour les y soumettre également. Cette décision de justice ne suit pas les conclusions de l’avocat général Bobek, publiées le 18 janvier de la même année, qui avait privilégié dans son analyse le critère de l’emploi d’ADN recombinant36. Elle élargit en revanche le champ d’application de la directive 2001/18/CE et y inclut les produits obtenus par édition du génome (OGE) car ils sont le résultat de techniques postérieures à l’année 2001 et mises en œuvre par l’homme, c’est-à-dire de manière « non naturelle ». Ce qui signifie que les variétés OGE devraient être soumises aux procédures européennes d’évaluation et d’étiquetage relatives aux OGM.
En rendant cette interprétation, la CJUE a fait « un choix radical, juridiquement absolument convaincant, en droite ligne avec l’impératif de précaution qui s’impose à l’Union » estiment les juristes Christine Noiville et Estelle Brosset37.
Elles précisent néanmoins que « dans le cadre d’une question préjudicielle, il ne lui [la CJUE] appartient pas de juger les faits, mais d’interpréter le droit de l’Union38» et que c’est aux autorités politiques de décider quelles sont les conditions pour qu’une « sécurité avérée » liée à l’utilisation d’OGM soit remplie…, ce qui renvoie immanquablement à l’interprétation du principe de précaution et au verrou qu’il constitue.
En France, le Conseil d’État ne s’est pas toujours prononcé sur l’application de cet arrêt, mais sa marge de manœuvre est étroite car, comme le constate Louis Boré, président de l’Ordre des avocats au Conseil d’État : « La relation entre le Conseil d’État et la Cour de Luxembourg ne relève pas d’un dialogue entre un maître et son élève, mais, en cas de bras de fer, ce sont toujours Luxembourg ou Strasbourg qui l’emporteront39. »
Une réglementation européenne sur les OGM lourde et coûteuse
La directive 2001/18/CE définit dans son annexe 1 ce qu’est un OGM et indique les techniques d’obtention qui seront soumises à la réglementation, c’est-à-dire celles qui seront considérées comme produisant des OGM réglementés et celles qui seront exclues du champ d’application bien que provoquant des modifications génétiques (mutagenèse, fusion cellulaire de cellules végétales « qui peuvent échanger du matériel génétique par des méthodes de sélection traditionnelles40»). Les critères déterminants pour être soumis à la réglementation sont l’utilisation de techniques qui provoquent l’incorporation de façon non naturelle de matériel génétique produit ou préparé hors de l’organisme dont le génome va être modifié, ou de méthodes non naturelles qui organisent une fusion cellulaire présentant de nouvelles combinaisons de matériel génétique41. Les techniques de transgénèse42 sont ainsi soumises à la directive 2001/18/CE.
Les dossiers de demande d’autorisation de commercialisation d’OGM à constituer sont volumineux. Les rubriques à renseigner doivent l’être de manière détaillée et nécessitent un investissement notable en termes d’expérimentations de laboratoire ou de terrain pour apporter les réponses demandées. De plus, quand est déposée une demande d’autorisation pour l’Europe (importation ou culture), il n’est pas toujours aisé pour le pétitionnaire de disposer de données pertinentes adaptées à la flore et à la faune européennes en raison des destructions d’expérimentations en champ par des opposants aux OGM, celles des pays où sont cultivées majoritairement les plantes transgéniques (continent américain) étant très différentes des pays européens.
Le dossier technique comprend un descriptif complet de la plante et de sa transformation incluant un dossier toxicologique complet (alimentarité, allergénicité, etc.). Il s’accompagne d’un plan d’évaluation des risques pour l’environnement précisant l’exposition et l’existence ou non de flux de gènes, de phénomènes de persistance et d’envahissement, d’éventuels effets immédiats, différés ou cumulés à long terme sur les organismes cibles et non cibles (faune, flore de l’environnement, les opérateurs), sur les cycles biogéochimiques et quelles sont les mesures prises pour les gérer.
Il doit enfin se conclure par un plan de surveillance postcommercialisation, qui comprend deux volets :
– une surveillance générale, qui vise à mettre en évidence des changements non prévisibles et des effets non intentionnels non connus sur des populations non cibles et non identifiées comme cibles potentielles : c’est ce que l’on appelle une surveillance non hypothesis-driven, non fondée sur des hypothèses. Cette démarche illustre parfaitement l’application pusillanime du principe de précaution ;
– une surveillance spécifique, destinée à mettre en évidence la survenue de changements attendus et à tester d’éventuelles hypothèses sur des effets négatifs de la plante transgénique liés à son utilisation dans l’environnement.
La surveillance postcommercialisation d’une plante transgénique est conduite sur la durée de l’autorisation de dix ans et donne lieu à des rapports annuels adressés à la Commission européenne via l’EFSA qui les fait expertiser par les États membres avant de rendre ses conclusions. Depuis 2011, l’EFSA demande que soit inclus dans le plan de surveillance postcommercialisation un volet d’études sur des situations critiques virtuelles et les risques encourus au moyen de scénarios43. En cas d’importation, une surveillance générale est aussi conduite pour détecter des anomalies entre les lieux de transbordement et de livraison des cargaisons.
Cette mobilisation considérable est très onéreuse (plus de 100 millions d’euros par dossier d’après les sociétés qui déposent des demandes d’homologation) pour détecter une anomalie incertaine et inconnue qui serait liée à la culture d’une plante transgénique. Seuls les grands conglomérats internationaux du secteur qui, par le biais de fusions-acquisitions, se sont formés depuis une vingtaine d’années (Corteva AgriScience, ChemChina et sa filiale Syngenta, Bayer qui a absorbé Monsanto44) ont l’assise financière suffisante pour assumer de telles exigences réglementaires spécifiques.
À ce dossier spécifique pour les OGM se surajoute la procédure normale de demande d’autorisation de mise sur le marché (AMM) d’une nouvelle variété végétale. En effet, quand on obtient une nouvelle variété sélectionnée par exemple pour une meilleure résistance à un bioagresseur (insecte ravageur ou agent pathogène) que ce soit par croisement classique, par mutagenèse ou par la transgénèse, elle devra être inscrite au « Catalogue officiel des espèces et variétés de plantes cultivées en France45» pour être commercialisée. Ces catalogues ont été établis afin de protéger l’acheteur (agriculteur, maraîcher, horticulteur, jardinier, etc.) en garantissant la conformité variétale et la qualité des semences qui sont vendues.
Pour être commercialisée, une nouvelle espèce ou variété de plantes doit satisfaire aux tests d’évaluation réalisés par le Groupe d’étude des variétés et des semences (Geves) qui consistent à vérifier la distinction, l’homogénéité et la stabilité (épreuves DHS) de la nouvelle variété mais aussi sa valeur agronomique, technologique et environnementale (épreuves VATE). C’est une procédure exigeante : sur un millier de variétés candidates examinées chaque année par le Geves, seules 30 à 40% satisfont aux épreuves DHS-VATE. Elle se déroule sous l’autorité du Comité technique permanent de la sélection (CTPS) qui propose au ministère de l’Agriculture l’inscription de la nouvelle variété au catalogue. C’est le ministère qui décide in fine de l’autorisation de mise sur le marché.
À l’été 2019, il existait plus de 9.000 variétés pour 190 espèces inscrites au catalogue français, et plus de 18.200 variétés d’espèces agricoles et 16.200 variétés d’espèces potagères inscrites au catalogue européen, qui regroupe tous les catalogues des États membres de l’Union européenne et de certains pays de l’Association européenne de libre-échange (AELE). Ainsi, au 24 juin 2019, si on se réfère à l’exemple du maïs, il existe 5.479 variétés inscrites au catalogue officiel européen des variétés de plantes, parmi lesquelles 150 portaient l’événement de transformation MON 810(46), actuellement le seul maïs transgénique cultivé dans l’Union européenne.
Dans ces conditions, il n’est pas étonnant que peu de sociétés soient capables de supporter les coûts de la commercialisation des OGM. Était-il légitime d’imposer cette lourde réglementation, très coûteuse, alors même qu’on avait très peu de recul sur cette technologie ? L’essayiste américain Jeremy Rifkin apporte la réponse cynique que la réglementation sur les OGM a d’abord été établie pour servir de garde-fou à d’éventuels procès en dommages et intérêts aux États-Unis47. Quoi qu’il en soit, des voix se font entendre aujourd’hui pour que cette réglementation soit allégée alors qu’aucun effet adverse majeur n’a été constaté dans les pays du monde cultivant les plantes biotech au cours de ces vingt dernières années.
Cette remise en cause est d’autant plus pertinente que, le 16 mai 2016, The National Academies of Sciences-Engineering-Medicine, qui regroupe les académies nationales des sciences, de l’ingénierie et de la médecine, a publié un rapport de plus 600 pages intitulé Genetically Engineered Crops. Experiences and Prospects. Sous la direction du professeur Fred Gould, vingt auteurs issus du monde académique ont réalisé un travail considérable, analysant plus de 1.000 publications scientifiques portant sur les plantes cultivées produites par génie génétique au cours des vingt dernières années, auditionnant 80 acteurs et recueillant 700 commentaires. Le comité a examiné longuement les effets agronomiques et environnementaux des mises en culture de plantes génétiquement modifiées, puis, dans un second volet, il s’est penché sur leurs effets sur la santé publique et a examiné les conséquences sociales et économiques de ces cultures. De ces travaux, il ressort que les plantes biotech mises en culture dans le respect des bonnes pratiques agricoles ne présentent pas plus de toxicité et d’écotoxicité, c’est-à-dire de risques sanitaires et environnementaux, que les plantes conventionnelles. Au contraire, elles peuvent améliorer la sécurité sanitaire et environnementale ainsi que les rendements. Ce rapport conclut en indiquant qu’au vu du débat sociétal, la question des plantes GM ne peut pas être examinée au seul prisme de la science mais doit prendre en compte les attentes des citoyens.
Quelle réglementation pour les OGE ?
La question d’une révision de la réglementation européenne appliquée aux OGM se pose d’autant plus aujourd’hui qu’elle devrait s’appliquer, selon l’arrêt de la CJUE du 25 juillet 2018, aux nouvelles techniques d’édition du génome. En conséquence, cet arrêt a été commenté par le groupe des conseillers scientifiques principaux qui compose le Scientific Advice Mechanism (SAM). Le 9 juin 2015, la Commission européenne a en effet créé un comité d’experts de haut niveau, de « sages » chargé de l’informer en toute indépendance et dans la transparence sur des sujets scientifiques afin d’élaborer en connaissance de cause les politiques de l’Union européenne. Les avis scientifiques donnés à la Commission doivent regrouper « les preuves et les idées provenant de différentes disciplines, être indépendant des intérêts institutionnels ou politiques, et doivent prendre en considération l’ensemble des politiques de l’Union48».
Dans une déclaration49, le comité souligne que « la directive OGM [2001/18/CE] stipule que “le cadre réglementaire créé pour les biotechnologies devrait être revu de façon à déterminer s’il est possible d’améliorer encore sa cohérence et son efficacité” ». Il considère par ailleurs que le contenu de l’arrêt de la Cour montre clairement qu’en raison des « nouvelles connaissances scientifiques et des récents progrès techniques, la directive OGM est désormais inadaptée ». Il remarque que « l’impossibilité les mutations apparaissant spontanément de celles qui résultent de différents types d’interventions humaines est une question importante du point de vue réglementaire » et insiste sur le fait que « ce sont les caractéristiques du produit final lui-même qui doivent être examinées indépendamment de la technique sous-jacente utilisée pour générer ce produit ». Ce conseil scientifique de haut niveau demande ainsi une révision de la réglementation européenne appliquée aux OGM, la considérant comme inadaptée aux NBT, notamment pour des raisons de contrôle et de traçabilité. Il insiste également sur la nécessité d’évaluer les caractéristiques du produit final et non de légiférer à partir de la méthode d’obtention. Il indique clairement que cette modification de la réglementation européenne existante doit tenir compte « des connaissances actuelles et les preuves scientifiques, en particulier sur l’édition génomique et les techniques établies de modification génétique » et que « cela devrait être fait en référence à d’autres réglementations relatives à la sécurité alimentaire et à la protection de l’environnement ». Afin de créer un environnement réglementaire favorable à l’innovation et que « la société puisse bénéficier des nouvelles sciences et technologies », il appelle au dialogue sociétal entre toutes les parties concernées et le grand public.
Actuellement, plusieurs pays sont en train de réviser la réglementation des plantes biotechnologiques :
– aux États-Unis, l’USDA a organisé une consultation publique (en cours) en indiquant que sa proposition « sustainable, ecological, consistent, uniform, responsible and efficient » (SECURE), c’est-à-dire « durabilité, écologie, de cohérence, uniformité, responsabilité et efficacité », doit moderniser la réglementation en matière de biotechnologie « avec une approche équilibrée qui continue de protéger la santé des végétaux tout en permettant aux innovations agricoles de prospérer50» ;
– au Japon, deux cas sont distingués : soit le produit final contient de l’ADN recombinant et il sera soumis à la réglementation des OGM, soit il n’en contient pas et ne sera pas considéré comme un OGM ;
– l’Australie ne réglementera pas les produits issus d’une modification du génome résultant de certaines techniques pour lesquelles le produit final se caractérise par une absence de séquence d’ADN exogène51 ;
Parmi les pays en développement, l’Argentine et le Brésil sont les plus avancés dans la réflexion :
– l’Argentine a opté pour une analyse au cas par cas ; un produit final sans transgène ne devrait pas être soumis à la réglementation des PGM mais un suivi spécifique pourrait être réalisé si des caractéristiques de la plante peuvent engendrer des risques pour la santé ou l’environnement ;
– le Brésil, effectuera des évaluations au cas par cas qui examineront les caractéristiques et la sécurité du produit final : dans ce cadre, la Comissão Técnica Nacional de Biossegurança (CTNBio) pourra dispenser de nouveaux produits OGE de l’évaluation réglementaire des OGM52 .
Le refus des OGM et des techniques d’édition du génome que professent certaines ONG et autres lobbyistes environnementalistes ne reposent pas sur des arguments scientifiques. Leur demander d’examiner le bilan des vingt dernières années afin de les convaincre que les bénéfices sont supérieurs aux risques est une démarche parfaitement illusoire. Les ONG qui sont de farouches opposants au développement des biotechnologies affichent clairement une opposition idéologique et politique à la société actuelle, et cette orientation est intervenue très tôt53.
Ainsi, dès 1986, après que les finances de l’ONG Greenpeace ont été mises à mal par l’arrêt des essais nucléaires français à Mururoa et par ses positions sur la guerre du Golfe54 (plus de 1 million de donateurs avaient cessé leurs contributions au mouvement), un groupe informel réuni en Europe autour d’Isabelle Meister et Arnaud Apotecker décide « que la lutte contre les OGM serait un thème porteur55». Ce groupe décida d’engager une campagne contre l’importation de soja transgénique américain en Europe. « Alerte au soja fou », titra ainsi le quotidien Libération du 1er novembre 1996. Ce titre faisait référence à la crise de la vache folle que connaissait l’Europe à cette époque et qui fut, d’après Marcel Kuntz, « la crise déterminante sur le destin des PGM en Europe56». Si, dans les années 1980-1990, les scandales qui se sont succédé (l’affaire du sang contaminé et la vache folle, entre autres) qui ont miné la confiance que le public avait dans les autorités publiques chargées de veiller à la sécurité sanitaire, la direction française de Greenpeace n’est pas pour autant convaincue que les OGM soient un danger pour la santé. La méfiance est ailleurs. Ainsi, Bernard Le Buanec rapporte les propos de Bruno Rebelle, directeur de Greenpeace France, en 2002 : « Nous n’avons pas peur des OGM. Nous sommes seulement convaincus qu’il s’agit d’une mauvaise solution. Les OGM sont peut-être une merveilleuse solution pour un certain type de société. Mais justement, c’est le projet de société dont nous ne voulons pas57.»
Quinze ans plus tard, les ONG anti-biotechnologies défendent toujours ce point de vue. L’association Les Amis de la terre déclare en 2016, à propos des NBT58 : « Le choix qui va être fait sur les nouvelles techniques va trancher pour ou contre un modèle sociétal qui cherche dans une fuite en avant technologique la solution pour les maux de la société de consommation débridée et le changement climatique. » Elle ajoute qu’il s’agit d’un refus de l’innovation et invoque le principe de précaution : « La décision qui doit être prise autour des nouvelles techniques est un choix politique et non technique. Est-ce que nous maintenons le principe de précaution ou est-ce que nous nous lançons dans une course effrénée et aveugle qui cherche le salut dans la nouveauté et dans une croyance inconditionnelle au progrès ? » Ce qui est en cause, ce n’est pas telle ou telle technique mais bien la société qui les développe.
Le débat est désormais clair. Les OGM et OGE, plus généralement les avancées biotechnologiques et les progrès qu’elles autorisent pour nourrir une population humaine en expansion démographique soutenue (2 milliards d’êtres humains de plus entre aujourd’hui et 2050, soit une estimation d’une population mondiale de 9,7 milliards d’habitants), pour améliorer le niveau et les conditions de vie des pays en développement et de leurs populations pauvres encore fortement agricoles, mais aussi pour s’adapter aux changements climatiques en favorisant l’innovation, ne sont pas en cause. Les groupements de pression anti-biotechnologies n’agissent pas sur des critères scientifiques et techniques mais refusent les biotechnologies par idéologie politique.
Conclusion
Sylvie Brunel, Toutes ces idées qui nous gâchent la Alimentation, climat, santé, progrès, écologie…, JC Lattès, 2019.
Quel avenir voulons-nous pour l’humanité ? Faut-il s’inscrire dans la collapsologie ambiante, « cette science du désastre qui fait recette et démobilise au lieu de nous galvaniser pour rechercher des solutions durables » comme la décrit Sylvie Brunel59 ? En écho à la citation de Rabelais qui ouvrait cette note, il faut, plus que jamais, se poser la question de savoir s’il est possible de croire en toute conscience à un avenir sans science.



















Aucun commentaire.